题目内容
下列物质按一定的分类方法,属于同一类的是( )
| A、标准状况下的状态:O2、CO2、H2O |
| B、酸性氧化物:SO2、Cl2O7、N2O5 |
| C、碱性氧化物:Na2O、CaO、Al2O3 |
| D、混合物:漂白粉、氯水、液氯 |
考点:酸、碱、盐、氧化物的概念及其相互联系,混合物和纯净物
专题:物质的分类专题
分析:A、标准状况下,H2O不是气态物质;
B、能和碱反应生成盐和水的化合物是酸性氧化物;
C、Al2O3是两性氧化物;
D、含有不同分子的物质是混合物.
B、能和碱反应生成盐和水的化合物是酸性氧化物;
C、Al2O3是两性氧化物;
D、含有不同分子的物质是混合物.
解答:
解:A、标准状况下,O2、CO2都是气体,但是H2O不是气态物质,故A错误;
B、SO2、Cl2O7、N2O5都能和碱反应生成盐和水,属于酸性氧化物,故B正确;
C、Al2O3是两性氧化物,Na2O、CaO属于碱性氧化物,故C错误;
D、漂白粉、氯水是含有不同分子的物质,是混合物,但是液氯属于纯净物,其中只含有氯气分子,故D错误.
故选B.
B、SO2、Cl2O7、N2O5都能和碱反应生成盐和水,属于酸性氧化物,故B正确;
C、Al2O3是两性氧化物,Na2O、CaO属于碱性氧化物,故C错误;
D、漂白粉、氯水是含有不同分子的物质,是混合物,但是液氯属于纯净物,其中只含有氯气分子,故D错误.
故选B.
点评:本题主要考查了物质的分类,注意概念的掌握和应用是关键,难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、由一种元素组成的物质可能是混合物 |
| B、同一主族不同元素的最高价氧化物,晶体结构一定相同 |
| C、最外层电子数为1的元素一定是主族元素 |
| D、由非金属元素组成的化合物一定是共价化合物 |
从同一瓶盐酸溶液中取任意体积时,下列物理量不随所取体积的多少而变化的是( )
| A、溶液中HCl的物质的量 |
| B、溶液的浓度 |
| C、溶液中Cl-的数目 |
| D、溶液的质量 |
下列说法①卢瑟福提出的“带核的原子结构模型”认为原子由位于原子中心的原子核和绕核作高速运动的核外电子构成②化学反应中原子之间通过电子转移都达到8电子稳定结构③1123Na的质量数为23,由该原子形成的钠离子的质量数也是23.其中正确的是( )
| A、①②③ | B、①② |
| C、①③ | D、只有① |
下列离子方程式书写正确的是( )
| A、向CuSO4溶液中加入钠:Na+Cu2+=Cu+Na+ |
| B、向Ba(OH)2溶液中滴加稀盐酸:2H++2Cl-+Ba2++2OH-=2H2O+BaCl2 |
| C、澄清石灰水与盐酸反应:H++OH-=H2O |
| D、往FeCl3溶液中加入Cu粉:2Fe3++3Cu=2Fe+3Cu2+ |
下列各项中,含氧原子数不同的是( )
| A、质量比为2:1的SO2和O2 |
| B、9g水和23g乙醇(C2H5OH) |
| C、标准状况下44.8L的一氧化氮和100 ml 5mol/L的硫酸溶液 |
| D、物质的量相同的Na2SO4和FeSO4 |
下列各组离子在指定环境中一定能大量共存的是( )
| A、在碳酸氢钠溶液中:K+、Al3+、SO42-、Cl- |
| B、存在较多Fe3+的溶液中:Na+、SCN-、CO32-、K+ |
| C、常温下由水电离出的C(H+)水?C(OH-)水=10-24溶液中:NH4+、Cl-、CO32-、F- |
| D、在能使pH试纸变深蓝色的溶液中:Na+、S2-、CO32-、NO3- |
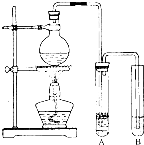 实验室制取少量溴乙烷的装置如图.
实验室制取少量溴乙烷的装置如图.