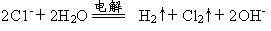题目内容
将1mol/L AlCl3溶液40mL与4mol/L NaOH溶液反应, 若产生0.01mol白色沉淀时, 消耗4mol/L NaOH溶液的体积为
[ ]
A.3mL B.7.5mL C.37.5mL D.15mL
答案:BC
解析:
解析:
|
①Al3+过量:
Al3++3OH- 3 1 4V 0.01 V=0.0075(L)(7.5mL) ②OH-过量
Al3++3OH- 1 3 1 1×0.04 4V 0.04
Al(OH)3──OH- 1 1 0.04-0.01 4V =0.03
V 共用NaOH的体积: 0.03+0.0075=0.0375(L) 即37.5(mL) |

练习册系列答案
相关题目
能正确表示下列反应的离子方程式为
A.用铁棒作阴极、炭棒作阳极电解饱和氯化钠溶液: |
| B.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32- +H2O |
| C.将1mol/L NaAlO2溶液和1.5mol/L的HCl溶液等体积互相均匀混合: 3AlO2-+ 6H+= 2 Al(OH)3↓+ Al3+ |
| D.NaClO溶液与FeCl2溶液混合:Fe2+ + 2ClO-+ 2H2O = Fe(OH)2↓ + 2HClO |