题目内容
 有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg
有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg| c(H+) |
| c(OH-) |
| A、A点时加入氢氧化钠溶液体积为20 mL |
| B、室温时0.01 mol?L-1的醋酸溶液pH=4 |
| C、OA段溶液中:c(CH3COO-)>c(CH3COOH) |
| D、若B点时加入NaOH溶液40 mL,所得溶液中:c(CH3COO-)+2 c(CH3COOH)=c(OH-)-c(H+) |
考点:中和滴定
专题:电离平衡与溶液的pH专题
分析:A、若加入氢氧化钠溶液体积为20 mL时,恰好生成醋酸钠溶液,醋酸钠溶液显碱性;
B、0.01mol?L-1的醋酸溶液AG=6;
C、OA段溶液中,加入少量NaOH时,溶液中主要是醋酸,醋酸的电离程度很小;
D、若B点时加入NaOH溶液40 mL,则c(Na+)=2[c(CH3COO-)+c(CH3COOH)],再结合电荷守恒分析.
B、0.01mol?L-1的醋酸溶液AG=6;
C、OA段溶液中,加入少量NaOH时,溶液中主要是醋酸,醋酸的电离程度很小;
D、若B点时加入NaOH溶液40 mL,则c(Na+)=2[c(CH3COO-)+c(CH3COOH)],再结合电荷守恒分析.
解答:
解:A、A点时AG=0,说明氢离子浓度 等于氢氧根离子浓度,溶液显中性,若加入氢氧化钠溶液体积为20 mL时,恰好生成醋酸钠溶液,醋酸钠溶液显碱性,故A错误;
B、0.01mol?L-1的醋酸溶液AG=6,说明c(H+)=10-4mol/L,c(OH-)=10-10mol/L,故B正确;
C、醋酸溶液中c(CH3COOH)>c(CH3COO-),故C错误;
D、若B点时加入NaOH溶液40 mL,则c(Na+)=2[c(CH3COO-)+c(CH3COOH)],据电荷守恒有c(CH3COO-)+c(OH-)=c(Na+)+c(H+),将c(Na+)=2[c(CH3COO-)+c(CH3COOH)]代入电荷守恒表达式,既可得c(CH3COO-)+2 c(CH3COOH)=c(OH-)-c(H+),故D正确;
故选BD.
B、0.01mol?L-1的醋酸溶液AG=6,说明c(H+)=10-4mol/L,c(OH-)=10-10mol/L,故B正确;
C、醋酸溶液中c(CH3COOH)>c(CH3COO-),故C错误;
D、若B点时加入NaOH溶液40 mL,则c(Na+)=2[c(CH3COO-)+c(CH3COOH)],据电荷守恒有c(CH3COO-)+c(OH-)=c(Na+)+c(H+),将c(Na+)=2[c(CH3COO-)+c(CH3COOH)]代入电荷守恒表达式,既可得c(CH3COO-)+2 c(CH3COOH)=c(OH-)-c(H+),故D正确;
故选BD.
点评:本题考查了醋酸钠溶液显碱性、pH计算、弱电解质的电离是微弱的、溶液中离子的守恒关系,题目难度较大.

练习册系列答案
相关题目
下列物质,属于电解质的是( )
| A、氯气 | B、乙醇 |
| C、食盐 | D、烧碱溶液 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、15g乙烷所含极性共价键的数目为3NA |
| B、0.1mol 甲基含有的质子数6.02NA |
| C、常温下,100mL0.1mol/L醋酸溶液中含醋酸分子为0.01NA |
| D、0.5mol乙醇完全燃烧时,转移的电子数为3NA |
下列有关硫的叙述中,不正确的是( )
| A、粘附在试管壁上的硫可用二硫化碳清洗 |
| B、S2和S8是同素异形体 |
| C、硫在自然界中主要以化合态形式存在 |
| D、硫粉和铜粉混合共热生成黑色的CuS |
以Mg、MgO、Mg(OH)2、MgCO3、MgSO4、BaCl2溶液和盐酸为原料,直接制取M可有多种方法,其中运用复分解反应的( )
| A、二种 | B、三种 | C、四种 | D、五种 |
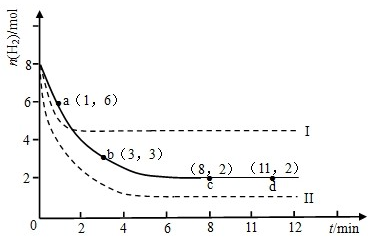 工业上“固定”和利用CO2能有效地减轻“温室’效应.有一种用CO2生产甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1
工业上“固定”和利用CO2能有效地减轻“温室’效应.有一种用CO2生产甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1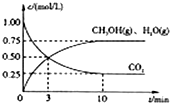 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.