题目内容
15.有关盐酸与氢氧化钠溶液反应的说法中,错误的是( )| A. | 属于复分解反应 | B. | 属于放热反应 | ||
| C. | 属于氧化还原反应 | D. | 属于中和反应 |
分析 盐酸与氢氧化钠溶液反应的化学方程式为HCl+NaOH=NaCl+H2O,属于酸碱中和反应,酸碱中和反应属于放热反应,属于复分解反应,所有的复分解反应都不是氧化还原反应.
解答 解:盐酸与氢氧化钠溶液反应的化学方程式为HCl+NaOH=NaCl+H2O,符合复分解反应发生的条件,属于复分解反应,所有的复分解反应都不是氧化还原反应,该反应属于酸碱中和反应,酸碱中和反应属于放热反应,
故选C.
点评 本题考查了化学反应的基本类型,难度不大,注意掌握四大基本反应类型与氧化还原反应的关系、常见的吸热反应和放热反应.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
5.关于酯的下列说法正确的是( )
| A. | 酯有刺激性气味 | B. | 油脂属于酯类 | ||
| C. | 酯难溶于水且密度大于水 | D. | 酯化反应中用NaOH溶液做催化剂 |
6.目前,CO、CO2的有效开发利用成为科学家研究的重要课题.
Ⅰ.CO可用于合成甲醇
(1)已知:CO、H2、CH3OH(g)的燃烧热分别为-283kJ•mol-1、-285.8kJ•mol-1、-764.5kJ•mol-1,则CO(g)+2H2(g)?CH3OH(g)的△H=-90.1kJ•mol-1.
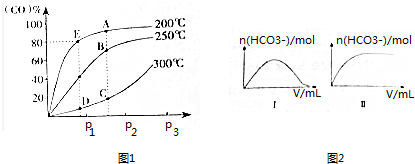
(2)将1molCO和2molH2充入密闭容器中发生上述反应.气体条件相同时,CO的平衡转化率[α(CO)]与压强(p)和温度(T)的关系如图1所示.
①A、B两点CH3OH的质量分数ω(A)>ω(B)(填“>”、“<”或“=”),理由为A点温度低于B点,该反应为放热反应,升高温度,平衡向逆反应方向移动.
②C、D两点的逆反应速率:v正(C)>v逆(D)(填“>”、“<”或“=”),理由为该反应为有气体参与的反应,C点压强大于D点,增大压强,反应速率越快.
③200℃时,测得E的容器容积为10L.该温度下,反应的平衡常数K=2500;保持温度和容积不变,再向容器中充入1molCO、1molH2和xmolCH3OH时,若使v正>v逆,则x的取值范围为0<x<58.
Ⅱ.CO2的综合利用
(3)CO2转化为甲醇有广泛应用前景.T℃时,在容积为1L的恒容密闭容器中,充入1molCO2和3molH2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,其它条件不变,下列措施中能使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大的是B(填选项字母).
A.升高温度 B.再充入1molCH3OH(g)和1molH2O(g) C.加入催化剂 D.再充入一定量CO2
(4)CO2可转化为碳酸盐,其中Na2CO3是一种用途广泛的碳酸盐.
已知:25℃时,几种酸的电离平衡常数如下表所示.
25℃时,向一定浓度的Na2CO3溶液中分别滴入等物质的量浓度的下列溶液至过量:①NaHC2O4②HNO3③HClO,溶液中的n(HCO3-)与所加入溶液体积(V)的关系如图2所示.其中,符合曲线Ⅰ的溶液为①②(填序号,下同);符合曲线Ⅱ的溶液为③.

Ⅰ.CO可用于合成甲醇
(1)已知:CO、H2、CH3OH(g)的燃烧热分别为-283kJ•mol-1、-285.8kJ•mol-1、-764.5kJ•mol-1,则CO(g)+2H2(g)?CH3OH(g)的△H=-90.1kJ•mol-1.
(2)将1molCO和2molH2充入密闭容器中发生上述反应.气体条件相同时,CO的平衡转化率[α(CO)]与压强(p)和温度(T)的关系如图1所示.
①A、B两点CH3OH的质量分数ω(A)>ω(B)(填“>”、“<”或“=”),理由为A点温度低于B点,该反应为放热反应,升高温度,平衡向逆反应方向移动.
②C、D两点的逆反应速率:v正(C)>v逆(D)(填“>”、“<”或“=”),理由为该反应为有气体参与的反应,C点压强大于D点,增大压强,反应速率越快.
③200℃时,测得E的容器容积为10L.该温度下,反应的平衡常数K=2500;保持温度和容积不变,再向容器中充入1molCO、1molH2和xmolCH3OH时,若使v正>v逆,则x的取值范围为0<x<58.
Ⅱ.CO2的综合利用
(3)CO2转化为甲醇有广泛应用前景.T℃时,在容积为1L的恒容密闭容器中,充入1molCO2和3molH2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,其它条件不变,下列措施中能使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大的是B(填选项字母).
A.升高温度 B.再充入1molCH3OH(g)和1molH2O(g) C.加入催化剂 D.再充入一定量CO2
(4)CO2可转化为碳酸盐,其中Na2CO3是一种用途广泛的碳酸盐.
已知:25℃时,几种酸的电离平衡常数如下表所示.
| H2CO3 | H2C2O4 | HNO2 | HClO |
| K1=4.4×10-7 K2=4.7×10-11 | K1=5.4×10-2 K2=5.3×10-5 | K=7.2×10-4 | K=2.9×10-8 |
20.已知下列两个热化学方程式:2H2(g)+O2(g)→2H2O(l)+571.6kJ,C3H8(g)+5O2(g)→3CO2(g)+4H2O(l)+2220.0kJ.实验测得,H2和C3H8的混合气体共10mol,完全燃烧放热7694kJ,则混合气体中H2和C3H8的体积比是( )
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 4:1 |
7.下列物质属于电解质的是( )
| A. | 铁线 | B. | 蔗糖 | C. | 氯化钠 | D. | 盐酸 |
5.在一定条件下,硫酸铵的分解反应为:4(NH4)2SO4=N2↑+6NH3↑+3SO2↑+SO3↑+7H2O,当有nmol电子转移时,下列说法正确的是( )
| A. | 有2nmol(NH4)2SO4分解 | B. | 有$\frac{n}{2}$molS原子被氧化 | ||
| C. | 生成$\frac{n}{6}$mol氧化产物 | D. | 生成7nmolH2O |
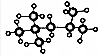 ,其分子式为:C8H18,A的一氯代物有4种;A有多种同分异构体,写出其中一氯代物只有一种同分异构体的结构简式(CH3)3CC(CH3)3;
,其分子式为:C8H18,A的一氯代物有4种;A有多种同分异构体,写出其中一氯代物只有一种同分异构体的结构简式(CH3)3CC(CH3)3;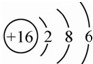 .
.