题目内容
 如图是某有机物的比例(填充)模型,该有机物的名称是( )
如图是某有机物的比例(填充)模型,该有机物的名称是( )| A、苯 | B、乙烷 | C、甲烷 | D、乙烯 |
考点:球棍模型与比例模型,常见有机化合物的结构
专题:有机化学基础
分析:比例模型可以直观地表示分子的形状,其碳原子的成键情况是确定分子结构的关键,碳原子的成键情况主要根据与碳原子形成共价键的原子的数目确定.
解答:
解:比例模型可以直观地表示分子的形状,其碳原子的成键情况是确定分子结构的关键,碳原子的成键情况主要根据与碳原子形成共价键的原子的数目确定.由此有机物的比例模型可知,一个该有机物分子含有两种原子H和C,每种原子的个数为6,分子式为C6H6,为平面正六边形结构,
故选:A.
故选:A.
点评:本题考查有机物分子的比例模型,学生利用模型得出有机物的结构简式是解答本题的关键,明确模型中不同小球代表的原子及成键来分析解答即可.

练习册系列答案
相关题目
某无色溶液能与铝反应放出氢气,该溶液中肯定不能大量共存的离子组是( )
| A、Na+、Fe2+、SO42-、K+ |
| B、HCO3-、K+、NO3-、SO42- |
| C、SO42-、Cl-、CO32-、Na+ |
| D、NH4+、Cl-、Na+、Ba2+ |
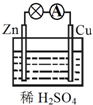 关于如图所示的原电池,下列说法不正确的是( )
关于如图所示的原电池,下列说法不正确的是( )| A、Cu为正极,Zn为负极 |
| B、该装置能将化学能转化为电能 |
| C、电子由铜片通过导线流向锌片 |
| D、正极反应为 2H++2e-═H2↑ |
下列化学反应既属于吸热反应又属于氧化还原反应的是( )
| A、生石灰溶于水 |
| B、焦炭与水蒸气的反应 |
| C、镁与稀盐酸反应 |
| D、氢氧化钡与氯化铵晶体混合 |
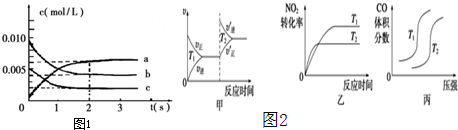 氮是大气中含量最多的气体,研究氮及其化合物对人类有重要的意义.
氮是大气中含量最多的气体,研究氮及其化合物对人类有重要的意义.