题目内容
已知:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1.现将一定量的稀盐酸、浓硫酸、稀醋酸分别和1L 1mol?L-1的NaOH溶液恰好完全反应,其中放热最少的是( )
| A、稀盐酸 | B、浓硫酸 |
| C、稀醋酸 | D、稀盐酸和稀醋酸 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1,中和热是强酸强碱稀溶液完全反应生成1mol水放出的热量,浓硫酸溶解过程中放热,醋酸是弱电解质存在电离平衡,电离过程是吸热过程.
解答:
解:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1,中和热是强酸强碱稀溶液完全反应生成1mol水放出的热量,一定量的稀盐酸和1L 1mol?L-1的NaOH溶液恰好完全反应放热57.3kJ;浓硫酸和1L 1mol?L-1的NaOH溶液恰好完全反应,溶解过程中放热,反应放热大于57.3kJ,醋酸是弱电解质存在电离平衡,电离过程是吸热程,醋酸和1L 1mol?L-1的NaOH溶液恰好完全反应放热小于57.3kJ.
故选:C.
故选:C.
点评:本题考查了中和热的概念分析判断,浓硫酸溶解放热,醋酸电离过程是吸热过程,题目较简单.

练习册系列答案
相关题目
化学与科学、技术、社会和环境密切相关.下列有关说法中错误的是( )
| A、对废旧电池进行回收处理 |
| B、研发使用高效催化剂,可提高反应中原料的转化率 |
| C、大力开发和应用氢能源有利于实现“低碳经济” |
| D、工业上,电解熔融MgCl2制金属镁 |
下列关于物质的鉴别、分离和提纯的说法中,正确的是( )
| A、HNO3溶液中混有H2SO4,可加入适量BaCl2溶液,过滤除去 |
| B、向某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成,说明该溶液中一定含有SO42- |
| C、向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
| D、不用其他任何试剂即可鉴别Ca(OH)2、Na2CO3与BaCl2三种无色溶液 |
下列说法中正确的是( )
| A、放热反应在常温下都能发生 |
| B、放热反应一定比吸热反应的反应速率快 |
| C、若某可逆反应的正反应放热,则逆反应一定是吸热 |
| D、吸热反应在任何条件下都不能自发进行 |
下列关于铝的叙述中正确的是( )
| A、铝合金是一种混合物,它比纯铝的熔点高 |
| B、由于铝的导电性比铜、银都强,所以常用其制造电线、电缆 |
| C、由于铝具有强还原性,所以可以通过铝热反应冶炼某些高熔点金属 |
| D、常温下,由于铝与浓硫酸钝化时不反应,所以可用铝制槽车运送浓硫酸 |
下列物质中属于强电解质的是( )
| A、盐酸 |
| B、BaSO4 |
| C、CH3COONa |
| D、H2O |
下列分子或离子在指定的分散系中能大量共存的一组是( )
| A、纯碱溶液:NH4+、K+、NO3-、NH3?H2O |
| B、空气:C2H2、CO2、SO2、NO |
| C、氢氧化铁胶体:H+、K+、S2-、Br- |
| D、高锰酸钾溶液:H+、Na+、SO42-、H2O2 |
电化学降解法治理水中硝酸盐的污染原理如图所示.下列说法正确的是( )
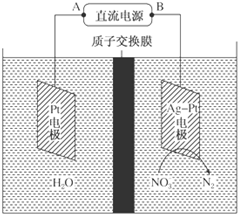

| A、B为电源正极 |
| B、电解过程中H+向阳极移动 |
| C、阴极反应式为2NO3-+6H2O+10e-=N2↑+12OH- |
| D、理论上电解过程中阴、阳两极产生的气体在同温同压下体积比为2:5 |