题目内容
15.氨是化肥工业和基本有机化工的主要原料,合成氨工业因此成为基本无机化工之一.回答下列问题:(1)如何获得廉价的氢气是合成氨工业中的重要课题,目前常用戊烷跟水蒸气反应的方法 获得氢气:
C5H12(g)+5H2O(g) $\frac{\underline{\;催化剂\;}}{高温}$5CO(g)+11H2(g)
已知几个反应的能量变化如图所示,则上述反应的△H=c-5a-11bkJ•mol-1
 (2)合成氨的反应原理为:
(2)合成氨的反应原理为:3H2(g)+N2(g) $?_{催化剂}^{高温高压}$2NH3(g)
现有甲、乙、丙3个固定容积为2L的密闭容器,在相同温度和催化剂条件下,按不同的反应物投入量进行合成氨反应,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol H2、2molN2 | 4mol H2、4molN2 | 2mol NH3 |
| 平衡时N2的浓度(mol•L-1) | c1 | 1.5 | C3 |
| 平衡时N2的体积分数 | w1 | W2 | W3 |
| 混合气体的密度(g•L-1) | ρ1 | ρ2 | ρ3 |
a.容器内混合气体的密度保持不变
b.3v正(N2)═v逆(H2)
c.容器内混合气体的平均相对分子质量保持不变
②乙容器中的反应在20min后达到平衡,这段时间内NH3的平均反应速率v(NH3)=0.05mol•L-1•min-1,该温度下,反应的平衡常数K=5.33L2•mol-2(结果保留3位有效数字);
③分析上表中的数据,下列关系正确的是ac(填序号).
a.cl>c3 b.wl<w2 c.ρ2>ρ1>ρ3
(3)在合成氨工业中,为了提高反应物的利用率,除了要提供适宜的温度、压强和使用催化剂外,还要采取的措施是将产物混合气中的氨冷却分离后,剩余气体循环使用.
分析 (1)由 可知:①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-aKJ•mol;②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-bKJ•mol;③C5H12(g)+8O2(g)=5CO2(g)+6H2O(g)△H=-cKJ•mol,由盖斯定律可知
可知:①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-aKJ•mol;②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-bKJ•mol;③C5H12(g)+8O2(g)=5CO2(g)+6H2O(g)△H=-cKJ•mol,由盖斯定律可知
C5H12(g)+5H2O(g) $\frac{\underline{\;催化剂\;}}{高温}$5CO(g)+11H2(g)△H=5①+11②-③;
(2)①化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再改变,由此衍生的一些物理量也不变,结合反应的特点进行分析;
②3H2(g)+N2(g) $?_{催化剂}^{高温高压}$2NH3(g)
初起(mol•L-1):2 2 0
变化(mol•L-1):1.5 0.5 1
平衡(mol•L-1):0.5 1.5 1
根据v=$\frac{△c}{△t}$计算,平衡常数等于平衡时生成物浓度幂之积比上反应物浓度幂之积;
③a.丙相当在甲的基础上减少氢气,平衡逆向移动,氮气的浓度增大,所以cl>c3;
b.乙相当在甲基础上增大压强,平衡正向移动,所以wl>w2;
c.根据ρ=$\frac{m}{V}$,体积相同,气体的质量越大密度越大,m乙>m甲>m丙,所以ρ2>ρ1>ρ3;
(3)将产物混合气中的氨冷却分离后,剩余气体循环使用,也可以使平衡正向移动,提高反应物的利用率.
解答 解:(1)由 可知:①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-aKJ•mol;②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-bKJ•mol;③C5H12(g)+8O2(g)=5CO2(g)+6H2O(g)△H=-cKJ•mol,由盖斯定律可知
可知:①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-aKJ•mol;②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-bKJ•mol;③C5H12(g)+8O2(g)=5CO2(g)+6H2O(g)△H=-cKJ•mol,由盖斯定律可知
C5H12(g)+5H2O(g) $\frac{\underline{\;催化剂\;}}{高温}$5CO(g)+11H2(g)△H=5①+11②-③=c-5a-11b,故答案为:c-5a-11b;
(2)①a.容器内混合气体的密度一直保持不变,不能作平衡的标志,故选;
b.3v正(N2)=v正(H2)═v逆(H2),达平衡状态,故不选;
c.容器内混合气体的平均相对分子质量保持不变,说明气体的物质的量不变,反应达平衡状态,故不选;故选a;
②3H2(g)+N2(g) $?_{催化剂}^{高温高压}$2NH3(g)
初起(mol•L-1):2 2 0
变化(mol•L-1):1.5 0.5 1
平衡(mol•L-1):0.5 1.5 1
根据v(NH3)=$\frac{△c}{△t}$=$\frac{1mol•{L}^{-1}}{20min}$=0.05mol•L-1•min-1,
K=$\frac{{1}^{2}}{0.{5}^{3}×1.5}$=5.33,故答案为:0.05mol•L-1•min-1,5.33;
③a.丙相当在甲的基础上减少氢气,平衡逆向移动,氮气的浓度增大,所以cl>c3,故正确;
b.乙相当在甲基础上增大压强,平衡正向移动,所以wl>w2,故错误;
c.根据ρ=$\frac{m}{V}$,体积相同,气体的质量越大密度越大,m乙>m甲>m丙,所以ρ2>ρ1>ρ3,故正确;
故选ac;
(3)将产物混合气中的氨冷却分离后,剩余气体循环使用,也可以使平衡正向移动,提高反应物的利用率,故答案为:将产物混合气中的氨冷却分离后,剩余气体循环使用.
点评 本题考查学生盖斯定律的应用、化学平衡移动及平衡常数与计算、合成氨条件的选择等,难度中等,关键是三行式的应用,要求学生要有扎实的基础知识和灵活应用知识解决问题的能力.

 名校课堂系列答案
名校课堂系列答案| A. | HCl+AgNO3═AgCl+HNO3 | B. | MnO2+4HCl(浓)═MnCl2+Cl2↑+H2O | ||
| C. | 2HCl$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑ | D. | Mg+2HCl═MgCl2+H2↑ |
| A. | Ba(OH)2溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| B. | CaCO3与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | NaHCO3溶液与NaOH溶液反应:HCO3-+OH-═CO32-+H2O | |
| D. | Cu与FeCl3溶液反应:Cu+Fe3+═Cu2++Fe2+ |
| A. | 在澄清透明的溶液中:H+、Na+、SO42-、Cu2+ | |
| B. | 在Kw/c(OH-)=1 mol•L-1的溶液中:Na+、NH4+、I-、CO32- | |
| C. | 在0.1 mol•L-1NaHSO4溶液中:K+、Fe2+、C1-、NO3- | |
| D. | 在能使甲基橙显黄色的溶液中:Ca2+、Ba2+、Br-、C1- |
| 选项 | |||
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状碳 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛有Na2SiO3溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至红色退去 | 2min后,试管里出现凝胶 | 非金属性:Cl>Si |
| C | 向盛有铜片的容器中加入浓硝酸 | 产生大量红棕色气体,溶液变为蓝绿色 | 浓硝酸具有强氧化性和酸性 |
| D | 向浓度均为KCl、KI混合溶液中滴加少量AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
| A. | 澄清的石灰水 | B. | 饱和碳酸钠溶液 | C. | 氯化钙溶液 | D. | 硝酸钡溶液 |
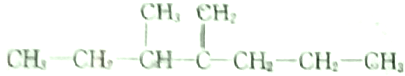 ,此烃名称为3-甲基-2-丙基-1-戊烯
,此烃名称为3-甲基-2-丙基-1-戊烯 ,可命名为1-甲基-3-乙基苯.
,可命名为1-甲基-3-乙基苯.