题目内容
(1)写出下列物质电子式:
S Al O2-
Mg2+ CaCl2 NH3
(2)用电子式表示下列物质形成过程:
Na2S:
CO2: .
S
Mg2+
(2)用电子式表示下列物质形成过程:
Na2S:
CO2:
考点:电子式,用电子式表示简单的离子化合物和共价化合物的形成
专题:化学键与晶体结构
分析:(1)书写原子的电子式时应把原子的最外层电子全部排列在元素符号周围,排列方式为在元素符号上、下、左、右四个方向,每个方向不能超过2个电子;
金属阳离子的电子式即为离子符号;
书写简单阴离子电子式,一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些电子都应画出,并将符号用“[]”括上,右上角标出所带的电荷数,电荷的表示方法同于离子符号;
离子化合物电子式的书写,分别写出阴阳离子,注意相同的离子不能合在一起书写;
共价化合物分析共用电子对情况;
(2)Na2S为离子化合物,2个钠原子各失去1个电子形成钠离子,1个硫原子得到2个电子形成硫离子;
CO2 为共价化合物,1个碳原子与2个氧原子共用4对电子.
金属阳离子的电子式即为离子符号;
书写简单阴离子电子式,一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些电子都应画出,并将符号用“[]”括上,右上角标出所带的电荷数,电荷的表示方法同于离子符号;
离子化合物电子式的书写,分别写出阴阳离子,注意相同的离子不能合在一起书写;
共价化合物分析共用电子对情况;
(2)Na2S为离子化合物,2个钠原子各失去1个电子形成钠离子,1个硫原子得到2个电子形成硫离子;
CO2 为共价化合物,1个碳原子与2个氧原子共用4对电子.
解答:
解:(1)S的电子式为: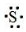 ; Al电子式为:
; Al电子式为: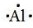 ;O2-电子式为:
;O2-电子式为: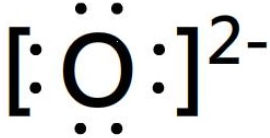 ;
;
Mg2+的电子式为Mg2+; CaCl2电子式为: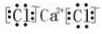 ;NH3
;NH3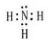 ;
;
故答案为: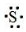 ;
;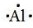 ;
;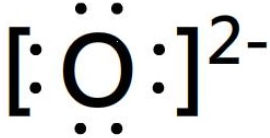 ;Mg2+;
;Mg2+;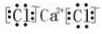 ;
;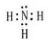 ;
;
(2)Na2S形成的过程: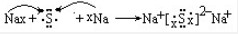 ;
;
二氧化碳形成的过程: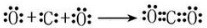 ;
;
故答案为: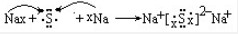 ;
;
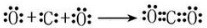 .
.
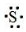 ; Al电子式为:
; Al电子式为: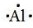 ;O2-电子式为:
;O2-电子式为: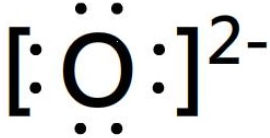 ;
;Mg2+的电子式为Mg2+; CaCl2电子式为:
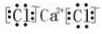 ;NH3
;NH3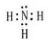 ;
;故答案为:
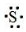 ;
;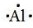 ;
;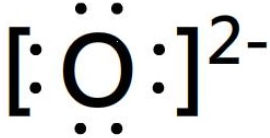 ;Mg2+;
;Mg2+;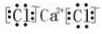 ;
;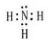 ;
;(2)Na2S形成的过程:
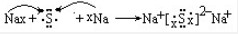 ;
;二氧化碳形成的过程:
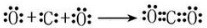 ;
;故答案为:
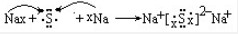 ;
;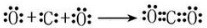 .
.
点评:本题考查了电子式的书写,注意掌握电子式的概念及表示方法,明确离子化合物与共价化合物的电子式的表示方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,11.2L CH2Cl2中含有的分子数为0.5NA |
| B、2.3g钠与足量氧气反应,转移的电子数为0.1 NA |
| C、1 mol甲基中含有的电子数为10NA |
| D、2.7g铝与足量氢氧化钠溶液反应转移的电子数NA |
在常温下,将0.1mol?L-1的CH3COONa溶液加水稀释,下列说法错误的是( )
| A、c(CH3COOH)增大 |
| B、溶液中c(H+)增大 |
| C、水解程度增大 |
| D、溶液的导电能力减弱 |



 △H=
△H=