题目内容
Ⅰ.对于下列氧化还原反应,请按要求填空.
(1)Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
①氧化剂是 ②离子方程式
(2)2H2S+SO2═3S↓+2H2O
①用双线桥法标出电子转移的方向和数目
②若氧化产物比还原产物多1.6g,则反应中电子转移的个数为
(3)请在下面用“单线桥法”表示该反应中电子转移的方向和数目.
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
Ⅱ.已知:将SO2通入FeCl3溶液中,溶液颜色会变为浅绿色,其原理可表示为:
□Fe3++□SO2+□H2O--□Fe2++□SO42-+□H+
(1)请配平上述离子方程式 ;
(2)已知向Fe2+溶液中滴加少量氯水时,溶液由浅绿色变为黄色.则Fe3+、SO2、Cl2的氧化性强弱顺序为 .
(1)Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
①氧化剂是
(2)2H2S+SO2═3S↓+2H2O
①用双线桥法标出电子转移的方向和数目
②若氧化产物比还原产物多1.6g,则反应中电子转移的个数为
(3)请在下面用“单线桥法”表示该反应中电子转移的方向和数目.
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
Ⅱ.已知:将SO2通入FeCl3溶液中,溶液颜色会变为浅绿色,其原理可表示为:
□Fe3++□SO2+□H2O--□Fe2++□SO42-+□H+
(1)请配平上述离子方程式
(2)已知向Fe2+溶液中滴加少量氯水时,溶液由浅绿色变为黄色.则Fe3+、SO2、Cl2的氧化性强弱顺序为
考点:氧化还原反应
专题:氧化还原反应专题
分析:I.(1)N元素的化合价降低,离子反应中只有硝酸、硝酸铜完全电离;
(2)2H2S+SO2═3S↓+2H2O中,S元素的化合价由-2价升高为0,S元素的化合价由+4价降低为0,该反应转移4e-,氧化产物、还原产物均为S,由反应可知,转移4mol电子时氧化产物比还原产物多32g,以此计算;
(3)2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合价由+7价降低为+2价,Cl元素的化合价由-1价升高为0,转移10e-;
Ⅱ.(1)Fe3+→Fe2+,化合价从+3→+2,降低1价,SO2→SO42-,化合价从+4→+6,升高2价,结合电子、电荷守恒分析;
(2)结合氧化剂的氧化性大于氧化产物的氧化性比较.
(2)2H2S+SO2═3S↓+2H2O中,S元素的化合价由-2价升高为0,S元素的化合价由+4价降低为0,该反应转移4e-,氧化产物、还原产物均为S,由反应可知,转移4mol电子时氧化产物比还原产物多32g,以此计算;
(3)2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合价由+7价降低为+2价,Cl元素的化合价由-1价升高为0,转移10e-;
Ⅱ.(1)Fe3+→Fe2+,化合价从+3→+2,降低1价,SO2→SO42-,化合价从+4→+6,升高2价,结合电子、电荷守恒分析;
(2)结合氧化剂的氧化性大于氧化产物的氧化性比较.
解答:
解:(1)①反应中N元素的化合价降低,则为氧化剂,故答案为:HNO3;
②离子反应中只有硝酸、硝酸铜完全电离,则离子反应为Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故答案为:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O;
(2)①2H2S+SO2═3S↓+2H2O中,S元素的化合价由-2价升高为0,S元素的化合价由+4价降低为0,该反应转移4e-,双线桥法标出电子转移的方向和数目为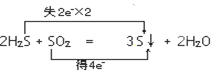 ,故答案为:
,故答案为: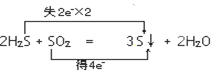 ;
;
②氧化产物、还原产物均为S,由反应可知,转移4mol电子时氧化产物比还原产物多32g,若氧化产物比还原产物多1.6g,则反应中电子转移的个数为
×4×NA=0.2NA个,故答案为:0.2NA;
(3)2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合价由+7价降低为+2价,Cl元素的化合价由-1价升高为0,转移10e-,“单线桥法”表示该反应中电子转移的方向和数目为 故答案为:
故答案为: ;
;
Ⅱ.(1)Fe3+→Fe2+,化合价从+3→+2,降低1价,SO2→SO42-,化合价从+4→+6,升高2价,由电子守恒可知铁元素前面系数为2,硫元素前面系数为1,则2Fe3++1SO2+H2O→2Fe2++1SO42-+H+,再根据氧原子守恒可知H2O前面系数为2,H+前系数为4,离子反应为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+;
(2)浅绿色为亚铁离子颜色,黄色为三价铁离子颜色,溶液由浅绿色变为黄色,说明亚铁离子被氧化为铁离子,故氧化性氯气强于三价铁离子,根据(1)可知,三价铁离子氧化性强于SO2,故答案为:Cl2>Fe3+>SO2.
②离子反应中只有硝酸、硝酸铜完全电离,则离子反应为Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故答案为:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O;
(2)①2H2S+SO2═3S↓+2H2O中,S元素的化合价由-2价升高为0,S元素的化合价由+4价降低为0,该反应转移4e-,双线桥法标出电子转移的方向和数目为
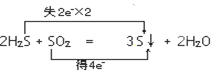 ,故答案为:
,故答案为: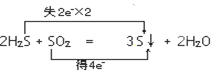 ;
;②氧化产物、还原产物均为S,由反应可知,转移4mol电子时氧化产物比还原产物多32g,若氧化产物比还原产物多1.6g,则反应中电子转移的个数为
| 1.6g |
| 32g |
(3)2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合价由+7价降低为+2价,Cl元素的化合价由-1价升高为0,转移10e-,“单线桥法”表示该反应中电子转移的方向和数目为
 故答案为:
故答案为: ;
;Ⅱ.(1)Fe3+→Fe2+,化合价从+3→+2,降低1价,SO2→SO42-,化合价从+4→+6,升高2价,由电子守恒可知铁元素前面系数为2,硫元素前面系数为1,则2Fe3++1SO2+H2O→2Fe2++1SO42-+H+,再根据氧原子守恒可知H2O前面系数为2,H+前系数为4,离子反应为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+;
(2)浅绿色为亚铁离子颜色,黄色为三价铁离子颜色,溶液由浅绿色变为黄色,说明亚铁离子被氧化为铁离子,故氧化性氯气强于三价铁离子,根据(1)可知,三价铁离子氧化性强于SO2,故答案为:Cl2>Fe3+>SO2.
点评:本题考查氧化还原反应,为高频考点,涉及配平及氧化性强弱比较、电子转移的方向和数目等,中等难度,注意配平一般用化合价升降法配平变价元素,再根据原子守恒配平其他元素,根据反应方程式判断氧化性,氧化剂的氧化性大于氧化产物的氧化性.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
下列各组原子结构示意图中,所表示的两种元素具有相似化学性质的是( )
A、 |
B、 |
C、 |
D、 |
如图的有机分子中不存在的官能团是( )


| A、碳碳双键 | B、醛基 |
| C、羧基 | D、羟基 |
下列叙述中错误的是( )
| A、乙烯的结构简式CH2CH2 |
B、甲醚的结构式 |
C、甲基的电子式为  |
D、苯甲酸乙酯的结构简式为  |
下列关于元素周期律的叙述正确的是( )
| A、随着元素原子序数的递增,原子最外层电子总是从1到8重复出现 |
| B、随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 |
| C、随着元素原子序数的递增,原子半径从小到大(稀有气体除外)发生周期性变化 |
| D、元素性质的周期性变化是指原子核外电子排布、原子半径及元素主要化合价的周期性变化 |
下列离子方程式书写正确的是( )
| A、锌和稀硝酸反应:Zn+2H+=Zn2++H2↑ |
| B、碳酸钡和盐酸反应:CO32-+2H+=CO2↑+H2O |
| C、氯气和过量的氢氧化钠溶液反应:Cl2+2OH-=Cl-+ClO-+H2O |
| D、氯化铝和过量的氨水反应:Al3++3OH-=Al(OH)3↓ |
 某烃A 0.2mol在氧气中充分燃烧后,生成化合物B、C各1.2mol,试回答:
某烃A 0.2mol在氧气中充分燃烧后,生成化合物B、C各1.2mol,试回答: 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题: