题目内容
标准状况下有①6.72LCH4;②3.01×1023个HCl分子;③17.6gCO2,下列对这三种气体的关系从大到小的排列顺序是:A.物质的量 B.气体体积 C.质量 D.电子数 E.密度 F.原子数 .
考点:物质的量的相关计算
专题:计算题
分析:①根据n=
计算的物质的量6.72L CH4,②根据n=
计算3.01×1023个HCl分子物质的量,根据n=
计算17.6gCO2 的物质的量,据此判断.
| V |
| Vm |
| N |
| NA |
| m |
| M |
解答:
解:①6.72L CH4的物质的量为
=0.3mol,
②3.01×1023个HCl分子的物质的量为
=0.5mol,
③17.6gCO2的物质的量为
=0.4mol
A、物质的量从大到小的排列顺序是:②>③>①,
B、气体体积与物质的量成正比,故气体体积从大到小的排列顺序是:②>③>①,
C、据m=n×M,①6.72LCH4质量为0.3mol×16g/mol=4.8g;②3.01×1023个HCl分子质量为0.5mol×36.5g/mol=18.25g,故质量从大到小的排列顺序是②>③>①,
D、电子数为质子数之和,①6.72LCH4电子物质的量为0.3mol×10=3mol;②3.01×1023个HCl电子物质的量为0.5mol×18=9mol,③17.6gCO2的电子物质的量为0.4mol×22=8.8mol,故电子数从大到小的排列顺序是:②>③>①,
E、密度与M成正比,M(CH4)=16,M(HCl)=36.5,M(CO2)=44,故密度从大到小的排列顺序是:③>②>①,
F、根据各物质分子中含有的原子数目,①6.72LCH4原子物质的量为0.3mol×5=1.5mol;②3.01×1023个HCl原子物质的量为0.5mol×2=1mol,③17.6gCO2的原子物质的量为0.4mol×3=1.2mol,故原子数从大到小的排列顺序是:①>③>②,
故答案为:②③①;②③①;②③①;②③①;③②①;①③②.
| 6.72L |
| 22.4L/mol |
②3.01×1023个HCl分子的物质的量为
| 3.01×1023 |
| 6.02×1023mol-1 |
③17.6gCO2的物质的量为
| 17.6g |
| 44g/mol |
A、物质的量从大到小的排列顺序是:②>③>①,
B、气体体积与物质的量成正比,故气体体积从大到小的排列顺序是:②>③>①,
C、据m=n×M,①6.72LCH4质量为0.3mol×16g/mol=4.8g;②3.01×1023个HCl分子质量为0.5mol×36.5g/mol=18.25g,故质量从大到小的排列顺序是②>③>①,
D、电子数为质子数之和,①6.72LCH4电子物质的量为0.3mol×10=3mol;②3.01×1023个HCl电子物质的量为0.5mol×18=9mol,③17.6gCO2的电子物质的量为0.4mol×22=8.8mol,故电子数从大到小的排列顺序是:②>③>①,
E、密度与M成正比,M(CH4)=16,M(HCl)=36.5,M(CO2)=44,故密度从大到小的排列顺序是:③>②>①,
F、根据各物质分子中含有的原子数目,①6.72LCH4原子物质的量为0.3mol×5=1.5mol;②3.01×1023个HCl原子物质的量为0.5mol×2=1mol,③17.6gCO2的原子物质的量为0.4mol×3=1.2mol,故原子数从大到小的排列顺序是:①>③>②,
故答案为:②③①;②③①;②③①;②③①;③②①;①③②.
点评:本题考查常用化学计量的有关计算,比较基础,注意对公式的理解与灵活运用,注意基础知识的掌握.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
下列化合物中同分异构体数目最少的是( )
| A、戊烷 | B、戊醇 |
| C、戊烯 | D、一氯戊烷 |
下列操作或发生事故时的处理方法正确的是( )
| A、浓硫酸不慎沾在皮肤上,应立即用大量水冲洗,再涂上3%~5%的小苏打溶液 |
| B、给试管里的液体加热时,试管应与桌面垂直 |
| C、配制一定物质的量浓度的NaCl溶液时,定容、振荡、摇匀后,发现液面低于刻度线,再加水到刻度线 |
| D、将pH试纸用蒸馏水润湿后,测定稀盐酸的pH值 |
下列有关说法中正确的是( )
| A、烧瓶、锥形瓶、量筒加热时均需垫上石棉网 |
| B、新制氯水保存在棕色细口瓶中,并放在阴凉处 |
| C、将蓝色硫酸铜晶体放入浓硫酸属于物理变化 |
| D、化石燃料属于可再生能源,不影响可持续发展 |
下列现象或事实可用同一原理解释的是( )
| A、铁分别加入浓硫酸和氢氧化钠溶液中均无明显现象 |
| B、SO2既能使品红褪色也能使酸性高锰酸钾褪色 |
| C、漂白粉溶液和硅酸钠溶液久置空中都变质 |
| D、H2O2溶液中加入MnO2或FeCl3溶液都能增大反应速率 |
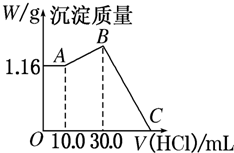 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得浊液中逐滴加入1.00mol?L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示.
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得浊液中逐滴加入1.00mol?L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示.