题目内容
(1)写出离子反应方程式H++OH-═H2O所对应的两个不同类型化学方程式.
① ;
② .
(2)写出下列反应的离子方程式
①氢氧化钠中通入过量二氧化碳
②铜与稀硝酸反应
(3)在下列反应中:
A.2F2+2H2O═4HF+O2
B.2Na+2H2O═2NaOH+H2↑
C.CaO+H2O═Ca(OH)2
D.2H2O
2H2↑+O2↑
水只做氧化剂的是 ,水只做还原剂的是 ,水既做氧化剂又做还原剂的是 ,水既不做氧化剂又不做还原剂的是 .请用单线桥法表示B反应的电子转移方向和数目 .
①
②
(2)写出下列反应的离子方程式
①氢氧化钠中通入过量二氧化碳
②铜与稀硝酸反应
(3)在下列反应中:
A.2F2+2H2O═4HF+O2
B.2Na+2H2O═2NaOH+H2↑
C.CaO+H2O═Ca(OH)2
D.2H2O
| ||
水只做氧化剂的是
考点:离子方程式的书写,氧化还原反应
专题:
分析:(1)可以是酸和碱的反应,也可以是盐和碱的反应;
(2)①二氧化碳过量,反应生成碳酸氢根离子;
②铜和稀硝酸反应生成硝酸铜、一氧化氮和水;
(3)从H2O中H、O元素的化合价是否发生变化,以及变化的趋势判断反应中H2O的作用,氧化还原反应中氧化剂得到电子,还原剂失去电子,以此书写反应的电子转移方向和数目.
(2)①二氧化碳过量,反应生成碳酸氢根离子;
②铜和稀硝酸反应生成硝酸铜、一氧化氮和水;
(3)从H2O中H、O元素的化合价是否发生变化,以及变化的趋势判断反应中H2O的作用,氧化还原反应中氧化剂得到电子,还原剂失去电子,以此书写反应的电子转移方向和数目.
解答:
解:(1)HCl+NaOH=NaCl+H2O,NaHSO4+NaOH=Na2SO4+H2O,二者反应的离子方程式都为H++OH-=H2O,所对应的两个不同类型化学物质的反应,
故答案为:HCl+NaOH=NaCl+H2O,NaHSO4+NaOH=Na2SO4+H2O;
(2)①过量二氧化碳通入氢氧化钠溶液中反应生成碳酸氢钠,该离子反应为:CO2+OH-=HCO3-,
故答案为:CO2+OH-=HCO3-;
②铜和稀硝酸反应生成硝酸铜、一氧化氮和水,反应的离子方程式为:3Cu+8H++2NO3-═3Cu2++2NO+4H2O,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO?+4H2O;
(3)A.2F2+2H2O=4HF+O2中,H2O中H元素化合价不变,O元素化合价升高,该反应中,H2O为还原剂;
B.2Na+2H2O=2NaOH+H2↑中,H2O中H元素的化合价降低,O元素化合价不变,该反应中,H2O为氧化剂;
C.CaO+H2O=Ca(OH)2 中,反应前后H、O元素的化合价不变,H2O既不作氧化剂又不作还原剂;
D.2H2O=2H2↑+O2↑ 中,H2O中H元素的化合价降低,O元素的化合价升高,H2O既作氧化剂又作还原剂,
在2Na+2H2O=2NaOH+H2↑中,Na是还原剂,2molNa失去2mol电子,水是氧化剂,得到2mol电子生成氢气,可表示为:
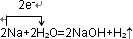 ,
,
故答案为B,A,D,C;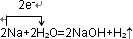 .
.
故答案为:HCl+NaOH=NaCl+H2O,NaHSO4+NaOH=Na2SO4+H2O;
(2)①过量二氧化碳通入氢氧化钠溶液中反应生成碳酸氢钠,该离子反应为:CO2+OH-=HCO3-,
故答案为:CO2+OH-=HCO3-;
②铜和稀硝酸反应生成硝酸铜、一氧化氮和水,反应的离子方程式为:3Cu+8H++2NO3-═3Cu2++2NO+4H2O,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO?+4H2O;
(3)A.2F2+2H2O=4HF+O2中,H2O中H元素化合价不变,O元素化合价升高,该反应中,H2O为还原剂;
B.2Na+2H2O=2NaOH+H2↑中,H2O中H元素的化合价降低,O元素化合价不变,该反应中,H2O为氧化剂;
C.CaO+H2O=Ca(OH)2 中,反应前后H、O元素的化合价不变,H2O既不作氧化剂又不作还原剂;
D.2H2O=2H2↑+O2↑ 中,H2O中H元素的化合价降低,O元素的化合价升高,H2O既作氧化剂又作还原剂,
在2Na+2H2O=2NaOH+H2↑中,Na是还原剂,2molNa失去2mol电子,水是氧化剂,得到2mol电子生成氢气,可表示为:
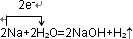 ,
,故答案为B,A,D,C;
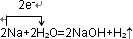 .
.
点评:本题考查离子方程式的书写以及氧化还原反应的应用等知识,题目难度中等,注意相关基础知识的积累,明确用双线桥、单线桥法分析氧化还原反应的方法.

练习册系列答案
相关题目
已知X、Y、Z、W是原子序数依次增大的短周期主族元素,X元素的最高价与最低负价代和等于2,Y的核电荷数是X的2倍,Z原子的K层和M层电子数之和与L层的电子数相等.下列说法不正确的是( )
| A、原子半径Y>Z>W |
| B、Y氧化物属于酸性氧化物 |
| C、对应的氢化物的热稳定性:W>Z |
| D、X的最高价氧化物对应的水化物弱酸 |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol Fe与足量的稀硝酸反应,转移3nA个电子 |
| B、常温下,16g CH4含有8nA个电子(相对原子质量:C-12,H-1) |
| C、0.5 mol?L-1Na2CO3溶液中含有nA个Na+ |
| D、标准状况下,22.4L氯水含有nA个Cl2分子 |
下列叙述中,正确的是( )
| A、H2O的摩尔质量是18 |
| B、等质量的O2和O3中所含的氧原子数相同 |
| C、常温下,22.4LNO2中所含的氧原子数为2NA |
| D、4gNaOH溶解于500mL水中,所得溶液的物质的量浓度为0.2mol?L-1 |
下列关于氯气或氯的化合物的叙述不正确的是( )
| A、过量的铁粉与氯气反应生成FeCl3 |
| B、少量SO2通入Ca(ClO)2溶液生成CaSO3沉淀 |
| C、氯气能使润湿的淀粉碘化钾试纸变蓝 |
| D、次氯酸钙比次氯酸稳定 |
下列关于药物使用的说法中,正确的是 ( )
| A、长期大量服用阿司匹林可预防疾病,没有毒副作用 |
| B、随着平价药房的开设,病人都可以到药店自行买药服用,不用到医院就诊 |
| C、随着平价药房的开设,病人都可以到药店自行买药服用,不用到医院就诊 |
| D、碘酒能使蛋白质变性,医院里常用于皮肤消毒. |
