题目内容
17.对于反应2P+4H2O2+2NaOH═Na2H2P2O6+4H2O,下列有关该反应说法正确的是( )| A. | P是氧化剂 | B. | 氧化性H2O2>Na2H2P2O6 | ||
| C. | 1mol H2O2反应,转移电子1mol | D. | Na2H2P2O6中磷元素的化合价为+3 |
分析 反应2P+4H2O2+2NaOH═Na2H2P2O6+4H2O中,磷元素由0价变成+4价,是还原剂,过氧化氢是氧化剂,1mol H2O2反应,转移电子2mol,结合氧化剂的氧化性强于氧化产物的氧化性分析判断.
解答 解:A、磷元素由0价变成+4价,是还原剂,故A错误;
B、过氧化氢是氧化剂,而Na2H2P2O6是氧化产物,所以氧化性H2O2>Na2H2P2O6,故B正确;
C、1mol H2O2反应,转移电子2mol,故C错误;
D、Na2H2P2O6中磷元素的化合价为+4,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子数的考查,注意从化合价分析,题目难度不大.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
7.某羧酸酯的分子式为C8H4O4,在酸性条件下1mol该酯完全水解可得到1mol醇和2mol乙酸,则符合要求的醇有(不考虑立体异构、同一个碳上连两个羟基的情况)( )
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
12.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 标准状况下,4.48 L水中含有的分子数目为0.2NA | |
| B. | 1 mol•L-1 的CaCl2溶液中,含有氯离子数2NA | |
| C. | 23g Na与足量O2反应转移的电子数为NA | |
| D. | 1mol苯中含有“C=C”的数目为3NA |
9.下列指定反应的离子方程式正确的是( )
| A. | 用氨水吸收足量的SO2气体:2OH-+SO2═SO32-+H2O | |
| B. | NaAlO2溶液中AlO2-的水解:AlO2-+2H2O═Al(OH)3↓+OH- | |
| C. | 加入NaClO将污水中的NH3氧化成N2:3ClO-+2NH3═N2↑+3Cl-+3H2O | |
| D. | NaHCO3溶液中加少量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
6.你认为减少酸雨产生的途径可采用的措施是:( )
①少用煤作燃料;②把工厂的烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新能源.
①少用煤作燃料;②把工厂的烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新能源.
| A. | ①②③ | B. | ②③④ | C. | ①③⑤ | D. | ③④⑤ |
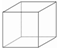 ,其六氯代物有3种;
,其六氯代物有3种;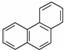 ,其二氯代物的数目为25种;
,其二氯代物的数目为25种;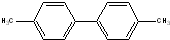 ),其二氯代物有16种.
),其二氯代物有16种.