题目内容
6.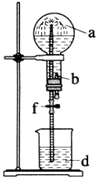 在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.a和b分别是( )
在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.a和b分别是( )| a(干燥气体) | b(液体) | |
| A | NO2 | 水 |
| B | CO2 | 水 |
| C | Cl2 | 饱和食盐水 |
| D | NH3 | 水 |
| A. | A | B. | B | C. | C | D. | D |
分析 解答时要从反应物和生成物的状态变化入手,注意到反应后气体减少或增多会引起气压的变化,则气体被吸收进溶液的反应,容器内气体减少,气压减小,a中的气体极易被b中试剂吸收或发生化学反应导致气压减小,以此来解答.
解答 解:A.NO2与水反应,生成硝酸和NO,容器内气体减少,气压减小,形成喷泉,但由于NO不溶于水,所以不会充满烧瓶,故A错误;
B.CO2与水的溶解度不大,锥形瓶与烧瓶内近乎压强相等,不能形成喷泉,故B错误;
C.氯气在饱和食盐水中的溶解度很小,锥形瓶与烧瓶内近乎压强相等,不能形成喷泉,故C错误;
D.NH3极易溶于水,烧瓶内压强减小为零,同外界大气压产生压强差,所以形成喷泉,并充满烧瓶,故D正确;
故选D.
点评 本题考查了喷泉实验,题目难度中等,明确喷泉实验的原理和各种气体的性质是解题关键,解题时注意把握化学和物理的联系,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
16.铁上镀铜时,电镀池的阴极为( )
| A. | 铜 | B. | 金 | C. | 石墨 | D. | 铁 |
17.下列说法正确的是( )
| A. | 将亚硫酸钠溶液在空气中蒸干、灼烧,得到的物质的主要成分是亚硫酸钠 | |
| B. | 硝酸亚铁溶液中加入一定量的盐酸可抑制Fe2+的水解,提高Fe2+的浓度 | |
| C. | 室温下OH-浓度相同的醋酸钠和碳酸钠的溶液加水稀释相同的倍数后,碳酸钠溶液的碱性弱 | |
| D. | 25℃,HCN的电离平衡常数Ka=5.0×10-10,同浓度的HCN和NaCN的混合溶液呈酸性 |
14.已知:(1)某无机高分子混凝剂的化学式可表示为Al2(OH)nClm•yH2O; (2)AgF+Cl2+H2O→AgCl+AgClO3+HF+O2(未配平).则( )
| A. | 混凝剂具有强氧化性 | |
| B. | Al2(OH)nClm•yH2O化学式中m等于3-n | |
| C. | 若(2)中Cl2化学计量数为a,则AgF的化学计量数为3a | |
| D. | 若(2)中AgClO3、O2的化学计量数分别为b、c,则AgCl的化学计量数为5b+4c |
1.等物质的量的氢气和氨气在同温同压下具有相等的( )
| A. | 原子数 | B. | 体积 | C. | 质子数 | D. | 质量 |
11.下列离子方程式的书写正确的是( )
| A. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | |
| B. | 向氯化亚铁溶液滴加新制氯水:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 铁和稀盐酸反应:2Fe+6H+═3H2↑+2Fe3+ |
15.下列试剂不能用于区分SO2和CO2的是( )
| A. | 澄清石灰水 | B. | 酸性高锰酸钾溶液- | ||
| C. | 溴水 | D. | 硝酸钡溶液 |
16.如图是某同学设计的验证原电池和电解池的实验装置,下列说法不正确的是( )
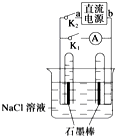

| A. | 若关闭K2、打开K1,一段时间后,发现左侧试管收集到的气体比右侧略多,则a为正极,b为负极 | |
| B. | 关闭K2,打开K1,一段时间后,用拇指堵住试管移出烧 杯,向试管内滴入酚酞,发现左侧试管内溶液变红色,则 a为负极,b为正极 | |
| C. | 若直流电源a为负极,b为正极,关闭K2,打开K1,一段时间后,再关闭K1,打开K2,则电路中电流方向为从右侧石墨棒沿导线到左侧石墨棒 | |
| D. | 若直流电源a为负极,b为正极,关闭K2,打开K1,一段时间后,再关闭K1,打开K2,则左侧石墨棒上发生的电极反应为H2-2e-+2OH-═2H2O |
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.