题目内容
下列排列顺序错误的是( )
| A、非金属性 As>S>Cl>F |
| B、金属性 Rb>K>Mg>Al |
| C、稳定性 PH3<H2S<HF |
| D、半径 Na>P>O>F |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.根据同周期元素从左到右非金属性逐渐增强,同主族元素从上到下非金属性逐渐增强判断;
B.根据同周期元素从左到右金属性逐渐减弱,同主族元素从上到下非金属性逐渐增强判断;
C.元素的非金属性越强,对应的氢化物越稳定;
D.根据同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大判断.
B.根据同周期元素从左到右金属性逐渐减弱,同主族元素从上到下非金属性逐渐增强判断;
C.元素的非金属性越强,对应的氢化物越稳定;
D.根据同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大判断.
解答:
解:A.同周期元素从左到右非金属性逐渐增强,同主族元素从上到下非金属性逐渐增强,则非金属性:As<S<Cl<F,故A错误;
B.根据同周期元素从左到右金属性逐渐减弱,同主族元素从上到下非金属性逐渐增强判断,则金属性 Rb>K>Mg>Al,故B正确;
C.元素的非金属性越强,对应的氢化物越稳定,非金属性:P<S<F,所以稳定性:PH3<H2S<HF,故C正确;
D.同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大,则半径:Na>P>O>F,故D正确;
故选A.
B.根据同周期元素从左到右金属性逐渐减弱,同主族元素从上到下非金属性逐渐增强判断,则金属性 Rb>K>Mg>Al,故B正确;
C.元素的非金属性越强,对应的氢化物越稳定,非金属性:P<S<F,所以稳定性:PH3<H2S<HF,故C正确;
D.同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大,则半径:Na>P>O>F,故D正确;
故选A.
点评:本题综合考查元素周期律知识,注意把握元素周期律的递变规律以及元素的金属性、非金属性与对应单质、化合物的关系,难度不大.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
对食物的酸、碱性判断正确的是( )
| A、西瓜是酸性食物 |
| B、猪肉、牛肉是碱性食物 |
| C、柠檬、橙是酸性食物 |
| D、苹果是碱性食物 |
下列离子方程式正确的是( )
| A、Zn和浓硫酸反应 Zn+2H+═H2↑+Zn2+ | ||
| B、钠与水反应:Na+2H2O═Na++2OH-+H2↑ | ||
C、硫酸铝溶液与过量氢氧化钠溶液反应:Al3++4OH-═AlO
| ||
D、向Ca(ClO)2溶液中通入少量CO2:ClO-+H2O+CO2═HClO+HCO
|
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是( )
| A、体积比为8:11 |
| B、密度之比为11:8 |
| C、物质的量之比为11:8 |
| D、原子个数之比为11:12 |
下列过程或事实不涉及氧化还原反应的是( )
①蔗糖炭化 ②用氢氟酸雕刻玻璃 ③铁遇冷的浓硫酸钝化 ④装碱液的试剂瓶不用玻璃塞 ⑤雷雨发庄稼 ⑥实际使用的浓硝酸显黄色.
①蔗糖炭化 ②用氢氟酸雕刻玻璃 ③铁遇冷的浓硫酸钝化 ④装碱液的试剂瓶不用玻璃塞 ⑤雷雨发庄稼 ⑥实际使用的浓硝酸显黄色.
| A、①③⑤⑥ | B、②④ |
| C、②③④⑥ | D、①②③④⑤⑥ |
乙炔在不同条件下可以转化成许多化合物,如图,下列叙述错误的是( )


| A、正四面体烷的二氯代物只有1种 |
| B、乙炔生成乙烯基乙炔是加成反应 |
| C、等质量的苯与乙烯基乙炔完全燃烧时的耗氧量不同 |
D、 与环辛四烯互为同分异构体 与环辛四烯互为同分异构体 |
一定量的硫酸与足量的锌粒发生反应,为减缓反应速率,且不影响生成氢气的总量,采取的措施有①改用等量锌粉、②加一定量的水、③加入适量KNO3溶液、④加CH3COONa固体、⑤加入NaOH溶液、⑥加热.其中正确的有( )
| A、②④ | B、②③④ |
| C、①⑥ | D、②③④⑤ |
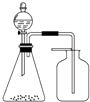 利用如装置能制取并收集到相应气体的是( )
利用如装置能制取并收集到相应气体的是( )| A、浓氨水与固体CaO制氨气 |
| B、浓盐酸与KClO3固体制氯气 |
| C、稀硝酸与铜片制NO |
| D、饱和食盐水与电石制乙炔 |
