题目内容
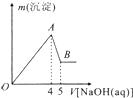 现有AlCl3和MgSO4的混合溶液,向其中不断加入NaOH溶液得到的沉淀的量与加入NaOH溶液的体积的关系如图所示,则原溶液中Cl-、SO42-的物质的量之比为( )
现有AlCl3和MgSO4的混合溶液,向其中不断加入NaOH溶液得到的沉淀的量与加入NaOH溶液的体积的关系如图所示,则原溶液中Cl-、SO42-的物质的量之比为( )| A、1:1 | B、3:2 |
| C、3:1 | D、6:1 |
考点:有关混合物反应的计算
专题:计算题
分析:氢氧化铝能和氢氧化钠反应而溶解,氢氧化镁不能溶于氢氧化钠中,则由图象可知,则4V~5体积时NaOH发生了NaOH与氢氧化铝的反应,由铝原子守恒可判断原溶液中的铝离子,即得出氯离子的量,再由0~4体积时NaOH发生镁离子、铝离子分别与碱反应生成沉淀,可确定镁离子的量,即得出硫酸根离子的量.
解答:
解:第一条上升的直线是表示AlCl3和MgSO4一起产生沉淀,第二条下降的直线表示Al(OH)3沉淀溶解,
设氢氧化钠溶液的浓度为c,
由第二条直线可知加入1体积的NaOH将氢氧化铝完全溶解,可知AlCl3是cmol,氯离子的量为3cmol,
这些氯化铝完全沉淀消耗氢氧化钠3体积,
再根据第一条直线可知,4-1×3=1体积的氢氧化钠将镁离子全部沉淀,
而2NaOH~MgSO4,所以MgSO4为0.5cmol,所以硫酸根离子的量为0.5cmol,
所以原溶液中Cl-与SO42-的物质的量之比为3cmol:0.5cmol=6:1,
故选D.
设氢氧化钠溶液的浓度为c,
由第二条直线可知加入1体积的NaOH将氢氧化铝完全溶解,可知AlCl3是cmol,氯离子的量为3cmol,
这些氯化铝完全沉淀消耗氢氧化钠3体积,
再根据第一条直线可知,4-1×3=1体积的氢氧化钠将镁离子全部沉淀,
而2NaOH~MgSO4,所以MgSO4为0.5cmol,所以硫酸根离子的量为0.5cmol,
所以原溶液中Cl-与SO42-的物质的量之比为3cmol:0.5cmol=6:1,
故选D.
点评:本题考查金属镁、铝的化合物的性质、有关混合物反应的计算,题目难度中等,注意氢氧化铝能和强碱反应是解题的关键所在,试题考查了学生的分析、理解能力及化学计算能力.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
如图是配制一定物质的量浓度溶液的过程示意图.下列说法中错误的是( )
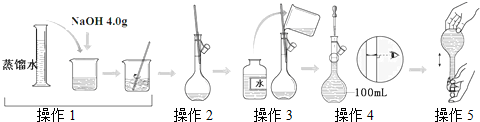

| A、所配制的NaOH溶液物质的量浓度为1.0 mol/L |
| B、操作2是将NaOH加水溶解后直接转移到容量瓶中 |
| C、操作4是滴加水至溶液凹液面的最低点与刻度线平齐 |
| D、操作5中,定容摇匀后发现液面低于刻度线,不能再继续加水 |
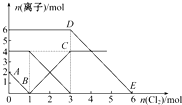 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-、2Fe3++2I-═2Fe2++I2,则下列有关说法中不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-、2Fe3++2I-═2Fe2++I2,则下列有关说法中不正确的是( )| A、还原性:I->Fe2+>Br- |
| B、线段AB表示Fe2+被氯气氧化 |
| C、线段BC表示生成4 mol Fe3+ |
| D、原溶液中n(Br-)=6 mol |
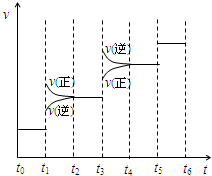
 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和如图表示:下列说法正确的是( )
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和如图表示:下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度 | T1 | T2 | T2 |
| 反应物 起始量 | 0.5molA 1.5molB | 0.5molA 1.5molB | 2.0molA 6.0molB |
| A、由图可知:T1<T2,且该反应为吸热反应 |
| B、T2时该反应的平衡常数K=0.8 |
| C、前10min乙、丙两容器中v(A)乙>v(A)丙 |
| D、C的质量m:m甲=m乙<2m丙 |

 氨气是一种重要的物质,可用于制取化肥和硝酸等.已知H-H键、N-H键、N≡N键的键能分别是436kJ/mol、391kJ/mol、946kJ/mol.
氨气是一种重要的物质,可用于制取化肥和硝酸等.已知H-H键、N-H键、N≡N键的键能分别是436kJ/mol、391kJ/mol、946kJ/mol.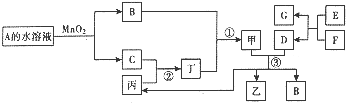 已知化合物A与B、丙与丁的组成元素相同,且四种物质中都含有同一种元素.A与B在常温下呈液态.D与F为常见金属单质,且D、F分别与甲的浓溶液分别在常温作用都无明显现象,加热时都有大量气体产生.E是一种红棕色粉末,A与丙可化合生成甲,乙、丙和B在常温下也可以生成甲和另一种化合物X,其部分转化关系如图(相关转化中部分反应条件和生成物未标出).
已知化合物A与B、丙与丁的组成元素相同,且四种物质中都含有同一种元素.A与B在常温下呈液态.D与F为常见金属单质,且D、F分别与甲的浓溶液分别在常温作用都无明显现象,加热时都有大量气体产生.E是一种红棕色粉末,A与丙可化合生成甲,乙、丙和B在常温下也可以生成甲和另一种化合物X,其部分转化关系如图(相关转化中部分反应条件和生成物未标出).