题目内容
10.接触法制硫酸中,进入接触室的气体必须净化、干燥,其主要原因是( )| A. | 防止催化剂中毒 | B. | 提高反应效率 | C. | 提高SO2转化率 | D. | 防止环境污染 |
分析 接触法制硫酸所用催化剂为V2O5,进入接触室的气体中含有与催化剂反应的气体,导致催化剂失效而中毒.
解答 解:从燃烧炉出来的气体叫做炉气.除去杂质和矿尘的目的是防止催化剂中毒,进行干燥的原因是防止水蒸气与二氧化硫形成酸对设备的腐蚀和在接触室里对催化氧化的不良影响.
故选A.
点评 本题考查工业制硫酸的知识,题目难度不大,注意工业制备硫酸的原理及设备.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
1.下列有关物质用途的叙述中,错误的是( )
| A. | 液氨常被用作制冷剂 | |
| B. | 可利用2Fe3++Cu═Cu2++2Fe2+腐蚀印刷电路板 | |
| C. | 为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质 | |
| D. | 已知3Cl2+8NH3═N2+6NH4Cl,工业上可用浓氨水检查氯气管道是否漏气 |
15.某KCl、MgCl2,、Mg(NO3)2形成的混合中,c(K+)=0.1mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.1mol/L,则c(NO3-)为( )
| A. | 0.15mol/L | B. | 0.10mol/L | C. | 0.25mol/L | D. | 0.40mol/L |
19.模拟电渗析法将海水淡化的工作原理示意图.己知X、Y均为惰性电极,模拟海水中富含Na+、Cl-、Ca2+、Mg2+、SO42-等离子.下列叙述中正确的是( )
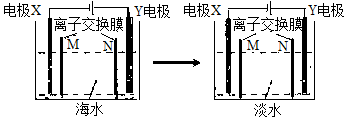

| A. | N是阴离子交换膜 | B. | Y电极上产生有色气体 | ||
| C. | X电极区域有浑浊产生 | D. | X电极反应式为4OH--4e-=O2↑+2H2O |
20.下列化学实验事实及其结论都正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 向纯碱中滴加足量浓盐酸,将产生的气体通入硅酸钠溶液,溶液变浑浊 | 酸性:盐酸>碳酸>硅酸 |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
| D | 取某溶液少量,加入盐酸酸化的氯化钡溶液,出现白色沉淀 | 该溶液中一定含有大量的SO42- |
| A. | A | B. | B | C. | C | D. | D |