题目内容
下列说法正确的是( )
| A、22.4LN2含阿伏加德罗常数个氮分子 |
| B、在标准状况下,22.4L水的质量约为18g |
| C、22g二氧化碳与标准状况下11.2LHCl含有相同的分子数 |
| D、在同温同压下,相同体积的任何气体单质所含的原子数相同 |
考点:阿伏加德罗常数,阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.没有告诉在标况下,不能使用标况下的气体摩尔体积计算氮气的物质的量;
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
C.22g二氧化碳的物质的量、标况下11.2L氯化氢的物质的量都是0.5mol;
D.不同的气体含有的原子数不一定相同,则含有的原子数不一定相等.
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
C.22g二氧化碳的物质的量、标况下11.2L氯化氢的物质的量都是0.5mol;
D.不同的气体含有的原子数不一定相同,则含有的原子数不一定相等.
解答:
解:A.不是标准状况下,不能使用标况下的气体摩尔体积计算22.4L氮气的物质的量,故A错误;
B.标况下水不是气体,不能使用标况下的气体摩尔体积计算11.4L水的物质的量,故B错误;
C.22g二氧化碳的物质的量为0.5mol,标况下11.2L氯化氢的物质的量为0.5mol,所以二者含有的分子数相同,故C正确;
D.同温同压下,相同体积的任何气体单质所含分子数相同,但是不一定含有相同的原子数,故D错误;
故选C.
B.标况下水不是气体,不能使用标况下的气体摩尔体积计算11.4L水的物质的量,故B错误;
C.22g二氧化碳的物质的量为0.5mol,标况下11.2L氯化氢的物质的量为0.5mol,所以二者含有的分子数相同,故C正确;
D.同温同压下,相同体积的任何气体单质所含分子数相同,但是不一定含有相同的原子数,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件是解答本题的关键,选项D为易错点,注意不同的气体分子含有的原子数可能不同.

练习册系列答案
相关题目
反应3X(g)+Y(g)?Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.1mol,则此反应的平均速率为( )
| A、v(X)=0.03 mol/(L?min) |
| B、v(Y)=0.02 mol/(L?min) |
| C、v(Z)=0.10 mol/(L?min) |
| D、v(w)=0.20 mol/(L?min) |
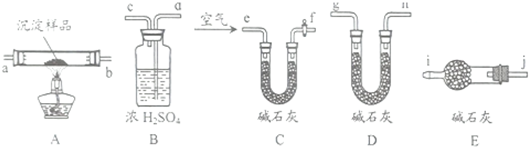
 如图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体,该装置可用于( )
如图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体,该装置可用于( )| A、二氧化锰和双氧水反应生成氧气 |
| B、浓氨水和生石灰混合生成氨气 |
| C、Na2SO3和浓H2SO4混合生成SO2 |
| D、锌粒与稀盐酸混合生成H2 |
下列说法正确的是( )
| A、常温下,铜与氧气很难反应,因为铜和氧气的反应是吸热反应 |
| B、金属锂在常温和加热情况下与氧气反应的产物不同 |
| C、焰色反应实验中的铂丝应用稀盐酸洗涤 |
| D、铝箔在空气中受热熔化,并不滴落,说明铝与氧气没有发生化学反应 |
在甲、乙两个密闭容器中,发生如下反应:2A(g)?B(g)+2C(s);△H=mkJ?mol-1.有如图两种图象.下列叙述正确的是( )


| A、若甲为恒容体系,图象(Ⅰ)代表温度不同时,时间与B的体积分数关系图,则m>0 |
| B、恒温条件下,图象 (Ⅰ)可能代表压强不同时,时间与B的体积分数关系图 |
| C、恒温条件下,若甲、乙两容器体积相同,起始时分别向甲中充入2molA,乙中充入1molB、3molC,则达到平衡后两容器中B的体积分数一定不同 |
| D、恒温条件下,乙容器存在图象 (Ⅱ)的关系,则当x代表压强时,y可代表B的体积分数 |
若N0代表阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下11.2LN2含有的分子数为0.5N0 |
| B、9mL水和标准状况下11.2L氮气含有相同的分子数(注水的密度为1g/mL) |
| C、同温同压下,N0个NO与N0个N2和02的混合气体的体积相等 |
| D、25℃、1.01×105Pa时,11.2L氧气所含的原子数目为N0 |
下列物质中,属于电解质的是( )
| A、氯化钾溶液 | B、澄清石灰水 |
| C、酒精 | D、氯化钠晶体 |