题目内容
将充满NO2和O2混合气体的量筒倒置于水中,充分反应后,保持气体压强不变,水进入至量简体积的一半处停止了,则原混合气体中NO2和O2的体积比是多少?
V(NO2):V(O2)= 2:3
解析:
NO2和O2的体积比不等于4:1,则需讨论 NO 2和O2分别过量时的两种情况。
设混合气体的体积为1,混合气体中NO2的体积为x,则O2为(1一x)
(1)假定原混合气体中V(NO2):V(O2)<4:l
4NO2+ O2+H2O=4HNO3
4 1
x x/4
剩余的O2:(1-x)-x/4=1/2解得x=2/3,V(NO2):V(O2)= 2:3
(2)假定原混合气体中NO2和O2的体积比>4:1
4NO2 + O2 +H2 O = 4HNO3
4 1
4(1-x) 1-x
暂时剩余NO2:1-5(1-x)=5x-4
由反应式②3NO2+H2O=2HNO3+NO 可知最后余NO:(5x-4)/3,由(5x-4)/3=1/2解得z=1.1(不合题意,舍去)

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
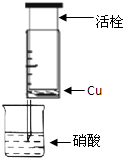 某研究性学习小组设计不同实验方案来研究硝酸的性质.
某研究性学习小组设计不同实验方案来研究硝酸的性质.