题目内容
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述中正确的是( )
| A、原子半径:A>B>D>C |
| B、原子序数:d>c>b>a |
| C、离子半径:C>D>B>A |
| D、元素的第一电离能:A>B>D>C |
考点:微粒半径大小的比较,元素周期律的作用
专题:化学键与晶体结构
分析:短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,所以有:a-2=b-1=c+3=d+1,且A、B在周期表中C、D的下一周期,原子序数:a>b>d>c,结合元素周期律递变规律解答该题.
解答:
解:短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,所以有:a-2=b-1=c+3=d+1,且A、B在周期表中C、D的下一周期,原子序数:a>b>d>c.
A.A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,原子核外电子层数越多,半径越大,同周期元素原子序数越大,半径越小,则有原子半径:B>A>C>D,故A错误;
B.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,所以有:a-2=b-1=c+3=d+1,所以原子序数:a>b>d>c,即A>B>D>C,故B错误;
C.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,核电荷数越大,离子半径越小,核电荷数a>b>d>c,所以离子半径C>D>B>A,故C正确;
D.非金属的第一电离能大于金属的第一电离能,金属性越强,第一电离能越小,则元素的第一电离能:B>A>C>D,故D错误;
故选C.
A.A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,原子核外电子层数越多,半径越大,同周期元素原子序数越大,半径越小,则有原子半径:B>A>C>D,故A错误;
B.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,所以有:a-2=b-1=c+3=d+1,所以原子序数:a>b>d>c,即A>B>D>C,故B错误;
C.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,核电荷数越大,离子半径越小,核电荷数a>b>d>c,所以离子半径C>D>B>A,故C正确;
D.非金属的第一电离能大于金属的第一电离能,金属性越强,第一电离能越小,则元素的第一电离能:B>A>C>D,故D错误;
故选C.
点评:本题考查元素周期表及微粒性质比较,为高频考点,把握核外电子排布确定元素所在周期表中的位置及元素性质的递变规律是解答该题的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某有机物6g与足量Na反应,生成0.05mol H2,该有机物可能是( )
| A、CH3CH2OH |
B、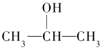 |
| C、CH3OH |
| D、CH3CH2COOH |
常温下,向20L真空容器中通入a mol H2S和b mol Cl2 (a、b都是正整数,且a≤5,b≤5),反应完毕后,容器内气体可能达到的最大密度是( )
| A、26.25 g?L-1 |
| B、18.25 g?L-1 |
| C、17.85 g?L-1 |
| D、12.05 g?L-1 |
把0.5molNa和0.5molMg分别投入到过量的m1g水和m2g盐酸中,分别得到溶液ma和mb.若m1=m2,则a与b的质量关系是( )
| A、ma>mb |
| B、ma<mb |
| C、ma=mb |
| D、无法确定 |
有关实验室用MnO2与盐酸反应制取氯气说法中,正确的是( )
| A、与制CO2一样,都用稀盐酸 |
| B、与制H2一样,可用向下排空气法收集 |
| C、与制O2一样,都需要加热 |
| D、与制O2一样,可用排水法收集 |
一氯代物有2种,二氯代物有4种的烃是( )
| A、丙烷 | B、2甲基丙烷 |
| C、丙烯 | D、苯 |
下列各组物质中,互为同分异构体的是( )
| A、白磷和红磷 |
| B、CH3CH2CH3和CH3CH2CH2CH3 |
| C、CH3CH(CH3)CH2CH3和CH3CH2CH(CH3)CH3 |
| D、CH3CH(CH3)CH2CH3和CH3CH2CH2CH2CH3 |
下列有关相对原子质量的叙述中,正确的是( )
| A、相对原子质量就是原子的质量 |
| B、氧的相对原子质量是16kg |
| C、相对原子质量是由质子数和电子数决定的 |
| D、相对原子质量与原子质量成正比 |
0.1mol两种气态烃组成的混合气体完全燃烧,得到0.16mol CO2和3.6g水,下列说法正确的是( )
| A、混合气体中可能有乙烷 |
| B、混合气体一定是甲烷和乙烯 |
| C、混合气体中一定有甲烷 |
| D、混合气体中一定有乙炔 |