题目内容
19.按要求填空(Ⅰ)①KOH的电子式
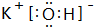 ②HClO的结构式H-O-Cl
②HClO的结构式H-O-Cl③乙醛在银镜反应中发生氧化反应(填氧化或还原)
(Ⅱ)3-对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
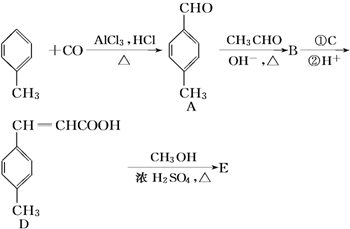
已知:R-CHO+CH3CHO$\underset{\stackrel{O{H}^{-},△}{→}}{\;}$ R-CH═CHCHO+H2O(R代表烃基)
(1)A的分子式为C8H8O,B中含氧官能团的名称为醛基
(2)试剂C可选用下列中的BC
A.溴水 B.银氨溶液 C.酸性KMnO4溶液 D.新制Cu(OH)2悬浊液
(3)写出D与甲醇(CH3OH)反应生成E的化学反应方程式
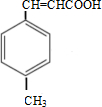 +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$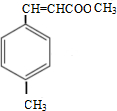 +H2O
+H2O(4)E在一定条件下可以生成高聚物F,F的结构简式为
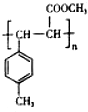 .
.
分析 (I)①KOH由钾离子与氢氧根离子构成;
②HClO中O原子与H原子、Cl原子之间分别形成1对共用电子对;
③乙醛在银镜反应中发生氧化反应;
(Ⅱ)由合成路线可知,甲苯与CO发生加成反应生成A,A与CH3CHO在碱性条件下反应生成B,B为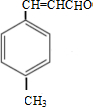 ,B中-CHO被氧化为-COOH,而碳碳双键不能被氧化,再酸化得到
,B中-CHO被氧化为-COOH,而碳碳双键不能被氧化,再酸化得到 ,则C为弱氧化剂,可以是新制氢氧化铜悬浊液或银氨溶液,D与甲醇发生酯化反应生成E为
,则C为弱氧化剂,可以是新制氢氧化铜悬浊液或银氨溶液,D与甲醇发生酯化反应生成E为 .
.
解答 解:(I)①KOH由钾离子与氢氧根离子构成,电子式为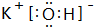 ,故答案为:
,故答案为: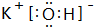 ;
;
②HClO中O原子与H原子、Cl原子之间分别形成1对共用电子对,结构式为H-O-Cl,故答案为:H-O-Cl;
③乙醛在银镜反应中发生氧化反应,故答案为:氧化;
(Ⅱ)由合成路线可知,甲苯与CO发生加成反应生成A,A与CH3CHO在碱性条件下反应生成B,B为 ,B中-CHO被氧化为-COOH,而碳碳双键不能被氧化,再酸化得到
,B中-CHO被氧化为-COOH,而碳碳双键不能被氧化,再酸化得到 ,则C为弱氧化剂,可以是新制氢氧化铜悬浊液或银氨溶液,D与甲醇发生酯化反应生成E为
,则C为弱氧化剂,可以是新制氢氧化铜悬浊液或银氨溶液,D与甲醇发生酯化反应生成E为 .
.
(1)A的分子式为C8H8O,B为 ,含氧官能团的名称为醛基,
,含氧官能团的名称为醛基,
故答案为:C8H8O;醛基;
(2)试剂C将醛基氧化为羧基,不能氧化碳碳双键,可以是银氨溶液或新制Cu(OH)2悬浊液,溴水能与碳碳双键发生加成反应,酸性高锰酸钾溶液可以氧化碳碳双键与羧基,
故答案为:BC;
(3)D与甲醇(CH3OH)反应生成E的化学反应方程式: +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$ +H2O,
+H2O,
故答案为: +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$ +H2O;
+H2O;
(4)E为 ,在一定条件下发生加聚反应生成高聚物F的结构简式为
,在一定条件下发生加聚反应生成高聚物F的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物推断与合成、有机物的结构与性质、常用化学用语等,熟练掌握官能团的性质与转化,是对有机化学基础的综合考查.

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案(1)用0.1mol/LNaOH溶液滴定体积均为20.00mL、浓度均为0.1mol/L盐酸和醋酸溶液,得到如下所示滴定曲线图:
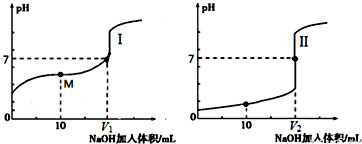
①用NaOH 溶液滴定醋酸溶液通常所选择的指示剂为酚酞,符合其滴定曲线的是I(填“I”或“II”);
②滴定前的上述三种溶液中,由水电离出的c(H+)最大的是CH3COOH溶液(填化学式);
③图中v1和v2大小的比较:v1<v2 (填“>”、“<”或“=”);
④图I中M 点对应的溶液中,各离子的浓度由大到小的顺序是c(CH3COO-)>c(Na+)>c(H+)>c(OH-).
(2)某同学为了研究难溶电解质的溶解平衡,设计了如下实验(相关数据测定温度及实验环境均为25℃):
| 操作步骤 | 现象 |
| 步骤1:向20mL0.05mol/LAgNO3溶液中加入20mL0.05mol/LKSCN溶液,充分反应后过滤 | 出现白色沉淀 |
| 步骤2:向滤液中加少量2mol/LFe(NO3)3溶液 | 溶液变红色 |
| 步骤3:向步骤2所得溶液中,加入少量3mol/LAgNO3溶液 | 现象a |
| 步骤4:取步骤1所得少量滤渣加入到适量的3mol/LKI溶液中 | 出现黄色沉淀 |
①请结合化学用语和必要的文字解释步骤2 现象出现的原因:由于存在沉淀溶解平衡AgSCN(s)?Ag+(aq)+SCN-(aq),溶液中仍有少量SCN-,Fe3+与SCN-结合生成Fe(SCN)3从而显红色.
②该同学根据步骤3中现象a推知,加入的AgNO3与步骤2所得溶液发生了反应,则现象a为出现白色沉淀,溶液红色变浅.
③写出步骤4 中沉淀转化反应平衡常数的表达式:K=$\frac{c(SC{N}^{-})}{c({I}^{-})}$.
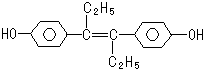
| A. | 它易溶于有机溶剂 | |
| B. | 该有机物可与少量Na2CO3反应放出CO2气体 | |
| C. | 1mol该有机物可以与5mol Br2发生反应 | |
| D. | 该有机物分子中,可能有16个碳原子共平面 |
| A. | 用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸 | |
| B. | 用食醋和澄清石灰水验证蛋壳中含碳酸盐 | |
| C. | 直接往淀粉水解液中滴入银氨溶液可产生银镜 | |
| D. | 用分液漏斗分离溴和苯 |

| A. | 将甲的溶液从t2℃降到t1℃,其溶质的质量分数一定减小 | |
| B. | t2℃时,甲、乙的饱和溶液各100g,其溶质的质量一定相等 | |
| C. | 当温度高于0℃而低于t1℃时,乙的溶解度比甲的溶解度大 | |
| D. | t2℃时,蒸发溶剂可使乙的饱和溶液析出晶体后变为不饱和溶液 |
| A. | 海水提镁的过程为:MgCl2(aq)$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{煅烧}{→}$MgO$\stackrel{电解}{→}$Mg | |
| B. | 石油裂化的主要目的是提高汽油等轻质燃油的产量 | |
| C. | 煤干馏的产品很多,属于化学变化 | |
| D. | 海水提溴是将海水中的化合态的溴富集再转化为游离态的溴 |
| A. | 第二周期 VIA族 | B. | 第三周期 VIA族 | C. | 第二周期ⅦA族 | D. | 第三周期 IVA族 |
| A. | OH- | B. | Mg2+ | C. | OD- | D. | D3O+ |
