题目内容
6.用a、b两个质量相等的Pt电极电解AlCl3和CuSO4的混合溶液[n(AlCl3):n(CuSO4)=1:9].t1时刻a电极得到混合气体,其中Cl2在标准状况下为 224mL(忽略气体的溶解);t2时刻Cu全部在电极上析出.下列判断正确的是( )| A. | a电极与电源的负极相连 | |
| B. | t2时,两电极的质量相差3.84 g | |
| C. | 电解过程中,溶液的pH不断增大 | |
| D. | t2时,b电极的电极反应是2H2O-4e-=2OH-+H2↑ |
分析 离子放电顺序为Cl->OH-,Cu2+>H+,t1时刻a电极得到混合气体,说明Cl-全部放电,得到的气体为Cl2和O2的混合物,n(Cl2)=$\frac{0.224L}{22.4L/mol}$=0.01mol,则n(AlCl3)=$\frac{2}{3}$×0.01mol,因n(AlCl3):n(CuSO4)=1:9,则n(CuSO4)=0.06mol,由于阴极只有Cu析出,则m(Cu)=0.06mol×64g/mol=3.84g,以此解答该题.
解答 解:A.a电极得到混合气体,为Cl2和O2的混合物,应为电解池的阳极,与电源的正极相连,故A错误;
B.n(Cl2)=$\frac{0.224L}{22.4L/mol}$=0.01mol,则n(AlCl3)=$\frac{2}{3}$×0.01mol,因n(AlCl3):n(CuSO4)=1:9,则n(CuSO4)=0.06mol,由于阴极只有Cu析出,则m(Cu)=0.06mol×64g/mol=3.84g,因此质量差即是产生的Cu的质量3.84g,故B正确;
C.电解过程中,由于OH-放电,则溶液H+浓度不断增大,溶液酸性增强,pH减小,故C错误;
D.t2时,Cu全部在电极上析出,电极反应为2H++2e-=H2↑,故D错误.
故选B.
点评 本题考查电解原题,注意把握离子的放电顺序,为解答该题的关键,根据电极反应进行计算和判断,题目难度中等.

练习册系列答案
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
16.单质铜及其化合物一般都具有特殊的颜色,如
某学校学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O,进行了认真的研究.
Ⅰ.查阅资料得出下列信息:
①Cu2O属于碱性氧化物; ②高温灼烧CuO生成Cu2O;
③Cu2O在酸性条件下能发生反应:Cu2O+2H+═Cu+Cu2++H2O.
Ⅱ.设计实验方案:
方案1:取该红色固体溶于足量的稀硝酸中,观察溶液颜色变化.
方案2:取该红色固体溶于足量的稀硫酸中,观察溶液是否呈蓝色.
方案3:称得干燥坩埚的质量为a g,取红色固体置于坩埚中称得总质量为b g,在空气中高温灼烧至质量恒定,称得最后总质量为c g.
(1)写出Cu2O与稀硝酸反应的化学方程式:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O.
(2)请你评价方案1和方案2的合理性,并简述理由:
方案1:不合理,因为铜和氧化亚铜均可溶于稀硝酸形成蓝色溶液.
方案2:合理,因为氧化亚铜与稀硫酸生成Cu和Cu2+,导致溶液呈蓝色.
(3)方案3中,若确认红色固体中含有Cu2O,则a、b、c的关系为c<$\frac{9b-a}{8}$,在该实验方案中最少应进行4次称量.
Ⅲ.学习小组乙设计了新的探究方案,拟根据干燥管中无水硫酸铜是否变蓝判断红色固体中是否含有Cu2O,装置如图所示.

(4)该探究方案中检验气体发生装置气密性的方法为:关闭活塞,从长颈漏斗向试管中注入一定量的水,使漏斗内液面高于试管内液面,静置后若漏斗内液面不下降,则装置的气密性良好;液面下降,则装置漏气;(说明操作方法、现象和结论).
(5)为确保探究的科学、合理和安全,你认为实验中还应采取的措施有ABC(填序号).
A.在氢气发生装置与硬质玻璃管之间增加一个干燥装置
B.加热前先排尽装置中的空气
C.在盛有无水硫酸铜的干燥管后再连接一个装有碱石灰的干燥管.
| Cu | Cu2O | CuO | Cu(OH)2 | CuSO4•5H2O |
| 红色(或紫红色) | 红色(或砖红色) | 黑色 | 蓝色 | 蓝色 |
Ⅰ.查阅资料得出下列信息:
①Cu2O属于碱性氧化物; ②高温灼烧CuO生成Cu2O;
③Cu2O在酸性条件下能发生反应:Cu2O+2H+═Cu+Cu2++H2O.
Ⅱ.设计实验方案:
方案1:取该红色固体溶于足量的稀硝酸中,观察溶液颜色变化.
方案2:取该红色固体溶于足量的稀硫酸中,观察溶液是否呈蓝色.
方案3:称得干燥坩埚的质量为a g,取红色固体置于坩埚中称得总质量为b g,在空气中高温灼烧至质量恒定,称得最后总质量为c g.
(1)写出Cu2O与稀硝酸反应的化学方程式:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O.
(2)请你评价方案1和方案2的合理性,并简述理由:
方案1:不合理,因为铜和氧化亚铜均可溶于稀硝酸形成蓝色溶液.
方案2:合理,因为氧化亚铜与稀硫酸生成Cu和Cu2+,导致溶液呈蓝色.
(3)方案3中,若确认红色固体中含有Cu2O,则a、b、c的关系为c<$\frac{9b-a}{8}$,在该实验方案中最少应进行4次称量.
Ⅲ.学习小组乙设计了新的探究方案,拟根据干燥管中无水硫酸铜是否变蓝判断红色固体中是否含有Cu2O,装置如图所示.

(4)该探究方案中检验气体发生装置气密性的方法为:关闭活塞,从长颈漏斗向试管中注入一定量的水,使漏斗内液面高于试管内液面,静置后若漏斗内液面不下降,则装置的气密性良好;液面下降,则装置漏气;(说明操作方法、现象和结论).
(5)为确保探究的科学、合理和安全,你认为实验中还应采取的措施有ABC(填序号).
A.在氢气发生装置与硬质玻璃管之间增加一个干燥装置
B.加热前先排尽装置中的空气
C.在盛有无水硫酸铜的干燥管后再连接一个装有碱石灰的干燥管.
17.某有机物的结构简式为HO-CH2CH=CHCH2-COOH.下列说法不正确的是( )
| A. | 它能与Na、NaOH、NaHC03等物质反应 | B. | 它能发生酯化、氧化、加成等反应 | ||
| C. | 该有机物分子式为C5H8O3 | D. | 它是乙酸也是乙醇的同系物 |
14.常温下,下列各组离子在指定的溶液中可能大量共存的是( )
| A. | 无色透明溶液中:Al3+、Ca2+、Cl-、HCO3- | |
| B. | 含大量Fe3+的溶液中:K+、I-、SO42-、NO3- | |
| C. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、SO32- | |
| D. | 由水电离出的c(H+)=1.0×10-14mol/L的溶液中:Mg2+、K+、Cl-、SO42- |
1.在下列4种化合物:①NaHCO3 ②Al2O3 ③(NH4)2S ④CH3COONH4中,跟盐酸和氢氧化钠溶液都能反应的是( )
| A. | 只有②④ | B. | 只有①② | C. | 只有①②③ | D. | ①②③④ |
11.下列有机物的系统命名正确的有( )
| A. | 2,3-二甲基-3,3-二乙基戊烷 | B. | 2-甲基-3-乙基丁烷 | ||
| C. | 2,2-二甲基-2-丁醇 | D. | 2,3-二甲基-1-丁醇 |
18.X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)Y的轨道表示式为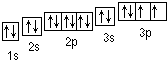 ;
;
(2)X、Y、Z三种元素的原子半径从大到小的顺序是S>Cl>C(用元素符号表示);
(3)XY2的分子中存在2个σ键,分子的空间构形为直线形,在H-Y、H-Z两种共价键中,键长较长的是H-S;
(4)W3+的核外电子排布式是1s22s22p63s23p63d5;
(5)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.此反应的化学方程式是2CO+SO2=S+2CO2;
(6)请设计一个实验方案,比较Y、Z单质氧化性的强弱在Na2S溶液中滴加Cl2水,若溶液出现浑浊,说明Cl2的氧化性比S强.
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为56,中子数为30 |
 ;
;(2)X、Y、Z三种元素的原子半径从大到小的顺序是S>Cl>C(用元素符号表示);
(3)XY2的分子中存在2个σ键,分子的空间构形为直线形,在H-Y、H-Z两种共价键中,键长较长的是H-S;
(4)W3+的核外电子排布式是1s22s22p63s23p63d5;
(5)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.此反应的化学方程式是2CO+SO2=S+2CO2;
(6)请设计一个实验方案,比较Y、Z单质氧化性的强弱在Na2S溶液中滴加Cl2水,若溶液出现浑浊,说明Cl2的氧化性比S强.
15.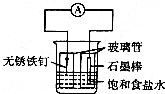 如图为铁的吸氧腐蚀实验装置,下列说法中错误的是( )
如图为铁的吸氧腐蚀实验装置,下列说法中错误的是( )
 如图为铁的吸氧腐蚀实验装置,下列说法中错误的是( )
如图为铁的吸氧腐蚀实验装置,下列说法中错误的是( )| A. | 右玻璃管内液面高于左玻璃管内液面 | |
| B. | 溶液中的Cl-向铁钉方向移动 | |
| C. | 石墨棒做正极,电极反应式为O2+2H2O+4e-═4OH- | |
| D. | 向插人铁钉的玻璃管内滴人Na0H溶液,可观察到铁钉附近的溶液中有沉淀生成 |
6.下列关于有机化合物的叙述中不正确的是( )
| A. | 丙烷跟甲烷一样能与氯气发生取代反应 | |
| B. | 相同条件,等物质的量的乙醇、乙二醇、丙三醇中分别加入足量的金属钠产生氢气的体积之比是2:3:6 | |
| C. | CH2Cl2只有一种结构说明甲烷是四面体结构而不是正方形结构 | |
| D. | 溴水既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷 |