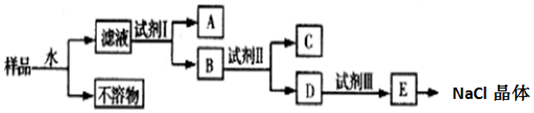
题目内容
15.25℃时,水电离的氢离子浓度和氢氧根离子浓度的乘积为10-12,则溶液一定为酸性×(判断对错)分析 常温下离子积常数10-14,25℃时,水电离的氢离子浓度和氢氧根离子浓度的乘积为10-12>10-14,水的电离被促进,是水解的盐溶液,可能显酸性或碱性.
解答 解:常温下离子积常数10-14,25℃时,水电离的氢离子浓度和氢氧根离子浓度的乘积为10-12>10-14,水的电离被促进,是水解的盐溶液,溶液可能显酸性或碱性,故答案为:×.
点评 本题考查了水电离平衡的影响因素、注意离子积常数的分析判断,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | CH4与C4H10不一定是同系物 | |
| B. | 苯分子中既含有碳碳单键,又含有碳碳双键 | |
| C. | 乙烯使溴水褪色属于取代反应 | |
| D. | 炒菜时,加入一点酒和醋能使菜味香可口,原因是有酯类物质生成 |
3.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 25℃时,pH=7的NH4Cl与NH3•H2O混合溶液:c(H+)=c(OH-)=c(NH4+)=c(Cl-) | |
| B. | 将pH=3的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| C. | 实验测得NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性:CH3COOH>H2CO3 | |
| D. | 0.01 mol•L-1Na2CO3溶液与0.01 mol•L-1NaHCO3溶液等体积混合:3[c(CO32-)+c(HCO3-)+c(H2CO3)]=2c(Na+) |
20.下列操作达不到预期目的是( )
①将CH4 通入氯水中制CCl4
②用溴水除去乙烯中混有的SO2气体
③用分液漏斗分离苯和甲苯的混合物
④将苯和溴水混合后加入Fe粉制溴苯.
①将CH4 通入氯水中制CCl4
②用溴水除去乙烯中混有的SO2气体
③用分液漏斗分离苯和甲苯的混合物
④将苯和溴水混合后加入Fe粉制溴苯.
| A. | 仅①④ | B. | 仅①③ | C. | 仅②③④ | D. | ①②③④ |
4.如图是探究铜丝与过量浓硫酸的反应,下列叙述不正确的是( )
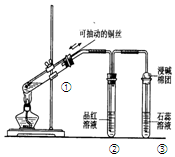

| A. | 上下移动①中铜丝可控制SO2的量 | |
| B. | ②中品红溶液褪色 | |
| C. | ③中石蕊溶液变红色 | |
| D. | 为确认CuSO4生成,向①中加水,观察溶液颜色 |
5.向含有c(FeCl3)=0.2mol•L-1、c(FeCl2)=0.1mol•L-1的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其中分散质粒子是直径约为9.3nm的金属氧化物,下列有关说法中正确的是( )
| A. | 该分散系是纯净物 | |
| B. | 可用过滤的方法将黑色金属氧化物与Na+分离开 | |
| C. | 加入NaOH时发生的反应可能为:Fe2++2Fe3++8OH-═Fe3O4+4H2O | |
| D. | 在电场作用下,阴极附近分散系黑色变深,则说明该分散系带正电荷 |
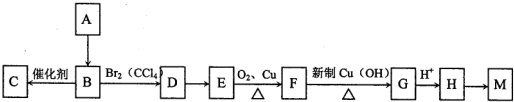
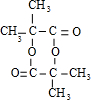 .
.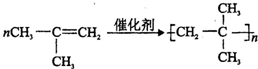 ;E→F
;E→F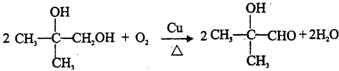 .
.