题目内容
7.下列说法正确的是( )| A. | 0.2mol/L与0.1mol/L醋酸中c(H+)之比为2:1 | |
| B. | pH=2与pH=1的硝酸中c(H+)之比为1:10 | |
| C. | 在50℃时,pH=2的硫酸与pH=12的NaOH溶液等体积混合后,溶液的pH=7 | |
| D. | pH均等于5的HCl溶液和NH4Cl溶液中,水的电离程度相等 |
分析 A.醋酸是弱电解质,浓度越小电离程度越大;
B.根据pH=-lgc(H+)计算出c(H+),据此计算判断;
C、在50℃时水的离子积不是1×10-14;
D、盐酸对水的电离起抑制作用,而氯化铵水解对水的电离起促进作用.
解答 解:A.醋酸是弱电解质,浓度越小电离程度越大,所以0.2mol/L与0.1mol/L醋酸中c(H+)之比小于2:1,故A错误;
pH=2的硝酸中c(H+)=10-2mol/L,pH=1的硝酸中c(H+)=10-1mol/L,二者氢离子浓度之比为10-2mol/L:10-1mol/L=1:10,故B正确;
C、在50℃时水的离子积不是1×10-14,所以pH=2的硫酸与pH=12的NaOH溶液等体积混合后,溶液的pH>7,故C错误;
D、盐酸对水的电离起抑制作用,而氯化铵水解对水的电离起促进作用,所以氯化铵溶液中水的电离程度大于盐酸,故D错误;
故选B.
点评 本题考查了溶液pH的计算方法,题目难度中等,明确溶液酸碱性与溶液pH的计算方法为解答关键,注意弱电解质部分电离的特点,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
17.如图是部分短周期元素最外层电子数与原子序数的关系图,下列说法正确的是( )


| A. | 原子半径:A<B<C<D | |
| B. | E、F和H三种元素相应的最高价氧化物对应水化物之间两两会发生反应 | |
| C. | 气态氢化物稳定性:D>I>G>H | |
| D. | E和C元素形成的化合物中只存在离子键 |
18.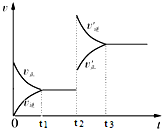 向一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g)△H<0,当达到平衡后,t2时刻改变反应的某一条件(混合气体总物质的量不变),速率变化如图所示,则下列说法正确的是( )
向一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g)△H<0,当达到平衡后,t2时刻改变反应的某一条件(混合气体总物质的量不变),速率变化如图所示,则下列说法正确的是( )
 向一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g)△H<0,当达到平衡后,t2时刻改变反应的某一条件(混合气体总物质的量不变),速率变化如图所示,则下列说法正确的是( )
向一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g)△H<0,当达到平衡后,t2时刻改变反应的某一条件(混合气体总物质的量不变),速率变化如图所示,则下列说法正确的是( )| A. | 重新达到平衡后,平衡常数K增大 | B. | t2时刻改变的条件可以是升高温度 | ||
| C. | I2(g)转化率增大,HI平衡浓度增大 | D. | t2时刻改变是可以增大压强 |
2.常温下,下列物质的水溶液,因为水解使溶液的pH<7的是( )
| A. | Na2S | B. | H2SO3 | C. | Al(SO4)3 | D. | NaHSO4 |
16.反应4P+3KOH+3H2O═3KH2PO2+PH3中磷单质发生的变化是( )
| A. | 只被氧化 | B. | 被氧化与被还原的个数比为1:3 | ||
| C. | 只被还原 | D. | 氧化剂与还原剂的质量比是1:3 |
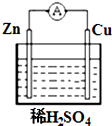 如图所示,在铜锌原电池中,以稀硫酸为电解质溶液:
如图所示,在铜锌原电池中,以稀硫酸为电解质溶液: