题目内容
(1)基态氮原子的价电子排布式是
(2)白磷分子的空间构型为
(3)金刚石的晶体结构中每个碳原子与周围的4个碳原子形成四个碳碳单键,这5个碳原子形成的是
1s22s22p3
1s22s22p3
.氮气分子中含有一个δ
δ
键,二个π
π
键.(2)白磷分子的空间构型为
正四面体
正四面体
,若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合6
6
个氧原子,若每个P原子上的孤对电子分别再以配位键连接一个氧原子,就可以得到磷的另一种氧化物P4O10
P4O10
(填分子式).(3)金刚石的晶体结构中每个碳原子与周围的4个碳原子形成四个碳碳单键,这5个碳原子形成的是
正四面体
正四面体
结构,金刚石晶体中C原子数与C-C键数之比为1:2
1:2
,晶体中最小的环上的碳原子数为6
6
.分析:(1)根据构造原理书写电子排布式,根据氮气的结构N≡N判断共价键类型和数目;
(2)白磷为正四面体结构,含有6个共价键,可形成化合物P4O10;
(3)在金刚石的晶体结构中每个碳原子与周围的4个碳原子形成四个碳碳单键,这5个碳原子形成的是正四面体结构,键角为109028,最小的环为6元环,结合均摊法计算C原子数与C-C键数之比.
(2)白磷为正四面体结构,含有6个共价键,可形成化合物P4O10;
(3)在金刚石的晶体结构中每个碳原子与周围的4个碳原子形成四个碳碳单键,这5个碳原子形成的是正四面体结构,键角为109028,最小的环为6元环,结合均摊法计算C原子数与C-C键数之比.
解答:解:(1)N原子的原子序数为6,基态氮原子的价电子排布式是1s22s22p3,氮气的结构式为N≡N,含有1个δ键,2个π键,
故答案为:1s22s22p3;δ;π;
(2)白磷为正四面体结构,含有6个共价键,若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合6个O原子,若每个P原子上的孤对电子分别再以配位键连接一个氧原子,还可结合4个O原子,则可形成化合物P4O10,
故答案为:正四面体;6;P4O10;
(3)金刚石晶体中每个C原子处于其他4个C原子构成的正四面体的内部,向周围无限延伸形成空间立体网状结构,最小的环是立体六元环,每个C原子周围有4条共价键,而每2个碳原子形成1个共价键,则金刚石晶体中C原子数与C-C键数之比为1:2,
故答案为:正四面体;1:2;6.
故答案为:1s22s22p3;δ;π;
(2)白磷为正四面体结构,含有6个共价键,若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合6个O原子,若每个P原子上的孤对电子分别再以配位键连接一个氧原子,还可结合4个O原子,则可形成化合物P4O10,
故答案为:正四面体;6;P4O10;
(3)金刚石晶体中每个C原子处于其他4个C原子构成的正四面体的内部,向周围无限延伸形成空间立体网状结构,最小的环是立体六元环,每个C原子周围有4条共价键,而每2个碳原子形成1个共价键,则金刚石晶体中C原子数与C-C键数之比为1:2,
故答案为:正四面体;1:2;6.
点评:本题考查较为综合,涉及晶胞的计算,电子排布式以及分子的立体构型等问题,题目难度中等,本题注意金刚石的结构特点,为易错点.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目

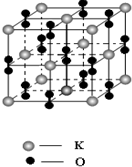 氧气是化工生产的重要原料,很多金属和非金属都能和氧气直接作用.
氧气是化工生产的重要原料,很多金属和非金属都能和氧气直接作用.



