题目内容
7.常温下氨能被Cl2、Br2、H2O2等氧化,已知以下反应:8NH3+3Cl2→6NH4Cl+N2(1)用单线桥标出电子转移的方向和数目.
(2)这一反应中,氧化剂是Cl2,氧化产物是N2.
(3)若有3mol N2生成,则发生氧化反应的物质有6mol.
(4)根据上述反应,若将浓氨水与Cl2靠近,将会看到白烟(现象).
分析 (1)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,氨气作还原剂,氯气作氧化剂;
(2)反应8NH3+3Cl2═6NH4Cl+N2中,氧化剂是氯气,氧化产物是氮气;
(3)若有3mol N2生成,则发生氧化反应的氨气为6mol;
(4)反应8NH3+3Cl2═6NH4Cl+N2中,所以将浓氨水与Cl2靠近,将会产生大量的白烟.
解答 解:(1)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,2molNH3作还原剂转移电子为6mol,则反应电子转移的方向和数目为 ,故答案为:
,故答案为: ;
;
(2)反应8NH3+3Cl2═6NH4Cl+N2中,氧化剂是氯气,氧化产物是氮气,故答案为:Cl2,N2;
(3)若有3mol N2生成,则发生氧化反应的氨气为6mol,故答案为:6mol;
(4)反应8NH3+3Cl2═6NH4Cl+N2中,所以将浓氨水与Cl2靠近,将会产生大量的白烟,故答案为:白烟. _
点评 本题考查氧化还原反应知识,侧重于氧化还原反应的计算,注意根据化合价的变化结合方程式判断氧化产物和还原产物的物质的量关系为解答该题的关键,题目难度不大.

练习册系列答案
相关题目
17.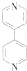 金属有机骨架材料(MOFs)为继碳纳米管后的又一种新型多孔材料.如图所示有机物可用于合成该材料,下列有关该有机物的说法不正确的是( )
金属有机骨架材料(MOFs)为继碳纳米管后的又一种新型多孔材料.如图所示有机物可用于合成该材料,下列有关该有机物的说法不正确的是( )
 金属有机骨架材料(MOFs)为继碳纳米管后的又一种新型多孔材料.如图所示有机物可用于合成该材料,下列有关该有机物的说法不正确的是( )
金属有机骨架材料(MOFs)为继碳纳米管后的又一种新型多孔材料.如图所示有机物可用于合成该材料,下列有关该有机物的说法不正确的是( )| A. | 6.8g该有机物含0.2 molN | |
| B. | 该有机物能发生加成反应 | |
| C. | 该有机物的一氯代物只有2种 | |
| D. | 分子中的所有原子可能处于同一平面 |
18.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,11.2L苯中含有C-H键的数目为3NA | |
| B. | 常温下,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| C. | 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| D. | 标准状况下22.4LSO3中含有的氧原子数目为3NA |
15.容量瓶上标有:(1)温度 (2)浓度 (3)容量 (4)压强 (5)刻度线这5项中的( )
| A. | (1)(2)(5) | B. | (1)(3)(5) | C. | (1)(4)(5) | D. | (2)(3)(4) |
2.下列除去杂质的方法正确的是(括号内的是杂质)( )
| A. | N2(CO):通过灼热的CuO粉末 | B. | Na2SO4溶液(Na2CO3):加盐酸 | ||
| C. | NaCl(NH4Cl):加热 | D. | NO2(NO):通入水中 |
12.某无色溶液中,可以大量共存的离子组是( )
| A. | Cu2+、Na+、NO3-、Cl- | B. | NH4+、K+、HCO3-、OH- | ||
| C. | Na+、Al3+、AlO2-、Cl- | D. | K+、Mg2+、SO42-、HCO3- |
16.A、B、C、D均属于短周期元素.A是元素周期表所有元素中原子半径最小的;B和C都只有两个电子层,B中一层电子数是另一层的两倍;C中两层电子数之和是两层电子数之差的两倍;D中一层电子数是另两层电子数之和,下列说法中正确的是( )
| A. | C的简单离子还原性大于D | |
| B. | D元素只能以化合态存在于自然界中 | |
| C. | A元素所形成离子的半径有可能大于He原子的半径 | |
| D. | B、D的原子不能相互结合形成化合物 |
17.某有机物的分子式为C9H12,其属于芳香烃的同分异构体有(不考虑、立体异构)( )
| A. | 5 种 | B. | 6 种 | C. | 7 种 | D. | 8 种 |
 和
和 .
.