题目内容
下列离子方程式的书写正确的是( )
| A、钠与水反应:Na+H2O═Na++OH-+H2↑ |
| B、用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O |
| C、AlCl3溶液中加入过量的浓氨水:Al3++3OH-═Al(OH)3↓ |
| D、Ba(OH)2溶液与H2SO4溶液混合:Ba2++SO42-+OH-+H+═BaSO4↓+H2O |
考点:离子方程式的书写
专题:
分析:A.电荷不守恒;
B.碳酸氢根离子与氢离子反应生成碳酸根离子和水;
C.一水合氨为弱电解质,应保留化学式;
D.离子个数不符合物质的配比.
B.碳酸氢根离子与氢离子反应生成碳酸根离子和水;
C.一水合氨为弱电解质,应保留化学式;
D.离子个数不符合物质的配比.
解答:
解:A.钠与水反应离子方程式:2Na+2H2O═N2a++2OH-+H2↑,故A错误;
B.用小苏打治疗胃酸过多,离子方程式:HCO3-+H+═CO2↑+H2O,故B正确;
C.AlCl3溶液中加入过量的浓氨水,离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故C错误;
D.Ba(OH)2溶液与H2SO4溶液混合,离子方程式:Ba2++SO42-+2OH-+2H+═BaSO4↓+2H2O,故D错误;
故选:B.
B.用小苏打治疗胃酸过多,离子方程式:HCO3-+H+═CO2↑+H2O,故B正确;
C.AlCl3溶液中加入过量的浓氨水,离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故C错误;
D.Ba(OH)2溶液与H2SO4溶液混合,离子方程式:Ba2++SO42-+2OH-+2H+═BaSO4↓+2H2O,故D错误;
故选:B.
点评:本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子方程式应遵循原子守恒、电荷守恒规律,题目难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
下列化学应用中不涉及氧化还原反应的是 ( )
| A、Na2S水溶液在空气中变浑浊 |
| B、生活中使用明矾净水,除去水中的悬浮颗粒 |
| C、溶有二氧化氮的浓硝酸做火箭的助燃剂 |
| D、漂白粉漂白有色布条 |
下列物质所含的化学键只有离子键的是( )
| A、H2O2 |
| B、CaF2 |
| C、KOH |
| D、Cl2 |
几种短周期元素的原子半径及主要化合价如下表:下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A、X元素在周期表中的位置是第三周期第Ⅱ族 |
| B、X和W能形成离子化合物 |
| C、Y的最高价氧化物对应的水化物能溶于稀氨水 |
| D、Z的氢化物的稳定性比W的氢化物的稳定性弱 |
“绿色化学”提倡化工生产应尽可能将反应物的原子全部利用,从根本上解决环境污染问题.在下列制备环氧乙烷的反应中,最符合“绿色化学”思想的是( )
A、 |
| B、CH2=CH2+Cl2+Ca(OH)2→CH2-CH2+CaCl2+H2O |
C、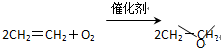 |
D、 |
下列措施对增大反应速率明显有效的是( )
| A、Na与水反应时增大水的用量 |
| B、将铝片改为铝粉,做铝与氧气反应的实验 |
| C、在K2SO4与BaCl2两溶液反应时,增大压强 |
| D、Fe与稀硫酸反应制取氢气时,改用浓硫酸 |
