��Ŀ����
��֪��H2(g)��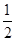 O2(g)=H2O(l) ��H1����285.8 kJ��mol��1 ��
O2(g)=H2O(l) ��H1����285.8 kJ��mol��1 ��
H2(g)=H2(l) ��H2����0.92 kJ��mol��1 �� O2(g)=O2(l) ��H3����6.84 kJ��mol��1 ��
H2O(g)=H2O(l) ��H4����44 kJ��mol��1 ��
����˵����ȷ����
A�������ĸ���Ӧ�������ȷ�Ӧ
B��1 molҺ̬H2����������1 mol��̬H2������
C��H2��ȼ����(��H)Ϊ��285.8 kJ��mol��1
D�������Һ��ȼ�յ��Ȼ�ѧ����ʽΪH2(l)��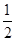 O2(l)=H2O(g) ��H����285.8 kJ��mol��1
O2(l)=H2O(g) ��H����285.8 kJ��mol��1
���𰸡�
C
��������
���������A.�ڢۢ�������״̬�ı仯��û�����������ɣ��������仯������B��������Һ̬ת��Ϊ��̬��Ҫ�������������1 molҺ̬H2������С��1
mol��̬H2������������C.
ȼ������1mol��������ȫȼ�ղ����ȶ��Ļ�����ʱ���ų���������Һ̬��ˮ���ȶ�״̬�������ȷ��D. ��-�ڡ�1/2- ��- �ܣ������ɵã�H2(l)��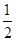 O2(l)=H2O(g) ��H����237.46kJ��mol��1.����
O2(l)=H2O(g) ��H����237.46kJ��mol��1.����
���㣺�����˹���ɵ�Ӧ�á��Ȼ�ѧ����ʽ����д��֪ʶ��

��ϰ��ϵ�д�
 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�
�����Ŀ
��ĿǰΪֹ���ɻ�ѧ��ת������ܻ������Ȼ������ʹ������Ҫ����Դ����ش��������⣺
��1��2C2H2��g��+5O2��g��=4CO2��g��+2H2O��l����H=-2599kJ?mol-1������Ȳ��ȼ����Ϊ ��
��2����Щ��Ӧ���еú�������Щ��Ӧ������ֱ�ӷ�������Щ��Ӧ�IJ�Ʒ�������и���Ӧ������������ⶨ��Ӧ����������ѣ���ʱ�����ø�˹���ɣ��Ϳ��Լ�ӵذ����ǵķ�Ӧ�ȼ����������֪
��CO��g��+
O2��g���TCO2��g����H1=-283.0kJ?mol-1
��C��s��+O2��g���TCO2��g����H2=-393.5kJ?mol-1
��C��s��+
O2��g��=CO��g����H= ��
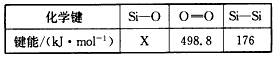
��3���ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̣���֪�������������
��ӦN2+3H2?2NH3��H=a kJ?mol-1���Ը��ݱ������м������ݹ���a= ��
��1��2C2H2��g��+5O2��g��=4CO2��g��+2H2O��l����H=-2599kJ?mol-1������Ȳ��ȼ����Ϊ
��2����Щ��Ӧ���еú�������Щ��Ӧ������ֱ�ӷ�������Щ��Ӧ�IJ�Ʒ�������и���Ӧ������������ⶨ��Ӧ����������ѣ���ʱ�����ø�˹���ɣ��Ϳ��Լ�ӵذ����ǵķ�Ӧ�ȼ����������֪
��CO��g��+
| 1 |
| 2 |
��C��s��+O2��g���TCO2��g����H2=-393.5kJ?mol-1
��C��s��+
| 1 |
| 2 |
��3���ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̣���֪�������������
| ��ѧ�� | ���ܣ�kJ/mol�� | ��ѧ�� | ���ܣ�kJ/mol�� |
| N��N | 942 | H-O | 460 |
| N-H | 391 | O=O | 499 |
| H-H | 437 |
 ��֪��H2��g��+
��֪��H2��g��+ ��֪��H2��g��+
��֪��H2��g��+