题目内容
核外电子数相同、所显电性和所带电量也相同的微粒称为等电子等质子体.下列各组内的两种微粒属于等电子等质子体的是( )
| A、Na+和Mg2+ |
| B、O2-和Mg2+ |
| C、F-和Cl- |
| D、Na+和NH4+ |
考点:质子数、中子数、核外电子数及其相互联系
专题:原子组成与结构专题
分析:根据右上角电荷数和元素种类确定核外电子数,所显电性和所带电量.
解答:
解:A.Na+所带电量为1个正电荷,Mg2+所带电量为2个正电荷,故A错误;
B.O2-和Mg2+所显电性不同,前者显负电性,后者显正电性,故B错误;
C.F-和Cl-核外电子数不同,前者为10个电子,后者为18个电子,故C错误;
D.Na+和NH4+核外电子数都为10个,都呈正电性,所带电量都为一个正电荷,故D正确;
故选D.
B.O2-和Mg2+所显电性不同,前者显负电性,后者显正电性,故B错误;
C.F-和Cl-核外电子数不同,前者为10个电子,后者为18个电子,故C错误;
D.Na+和NH4+核外电子数都为10个,都呈正电性,所带电量都为一个正电荷,故D正确;
故选D.
点评:本题主要考查了微粒中质子数和电子数的确定,难度不大,给出的微粒,会根据微粒的构成情况确定质子数和电子数.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
一定温度下在一容积恒定的密闭容器中,进行如下可逆反应:2A(g)+B(s)?C(g)+D(g).当下列物理量不再发生变化时,能表明该反应已达到平衡状态的是( )
①容器内混合气体的密度 ②容器内混合气体的压强 ③容器内混合气体的总物质的量 ④容器内C物质的物质的量浓度.
①容器内混合气体的密度 ②容器内混合气体的压强 ③容器内混合气体的总物质的量 ④容器内C物质的物质的量浓度.
| A、①④ | B、②③ | C、②③④ | D、④ |
下列物质属于均匀混合物的( )
①合金;②硝酸纤维素的乙醚溶液;③红褐色氢氧化铁胶体;④生理盐水.
①合金;②硝酸纤维素的乙醚溶液;③红褐色氢氧化铁胶体;④生理盐水.
| A、①②③④ | B、①② |
| C、②③ | D、③④ |
由一种阳离子与两种酸根离子组成的盐称为混盐.混盐CaOC12在酸性条件下可以产生C12,下列关于混盐CaOC12的有关判断不正确的是( )
| A、该混盐与硫酸反应产生1molC12时转移2NA个电子 |
| B、该混盐的水溶液呈碱性 |
| C、该混盐具有较强的氧化性 |
| D、该混盐中氯元素的化合价为+1和-1 |
如图所示是短周期的一部分,已知B原子与C 原子核外电子总数之和为A的4倍,则下列推断正确的是( )

| A、A、B、C三者中,A为金属性元素,B、C为非金属性元素 |
| B、A、B、C三者核电荷数之和为40 |
| C、A与B、A与C均可形成离子化合物 |
| D、B与C只能形成一种共价化合物 |
下列各离子方程书写正确的是( )
| A、H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| B、将氯化亚铁溶液和稀硝酸混合:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
| C、在FeI2溶液中通入少量的氯气:2Fe2++Cl2=2Fe3++2Cl- |
| D、Fe(OH)3与足量的HI溶液反应:Fe(OH)3+3H+=Fe3++3H2O |
下列化学用语能正确表示相应意义的是( )
| A、乙烯的结构简式C2H4 |
| B、丁烷的结构简式CH3(CH2)2CH3 |
C、四氯化碳的结构式 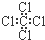 |
D、苯的分子式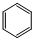 |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:下列说法错误的是( )
| 物质 | X | Y | Z |
| 初始浓度/mol/L | 1 | 2 | 0 |
| 平衡浓度/mol/L | 0.6 | 1.6 | 0.8 |
| A、增大压强使平衡向生成Z的方向移动,平衡常数增大 | ||
B、反应可表示为X+Y?2Z,其平衡常数为
| ||
| C、反应达到平衡时,Y的转化率为20% | ||
| D、改变温度可以改变此反应的平衡常数 |