题目内容
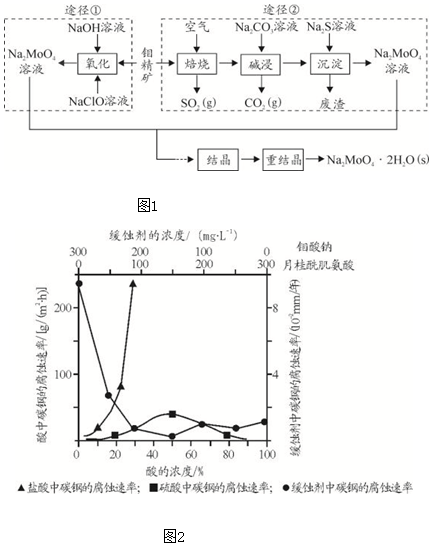
6. 短周期主族元素W、X、Y、Z的原子序数依次增大,Y和Z位于同一主族.m、n、p均为由这些元素组成的二元化合物,甲、乙、丙为其中三种元素对应的单质,丙为黄色固体,易溶在XZ2中,p是一种二元弱酸.上述物质的转化关系如图所示(反应条件省略).下列说法正确的是( )
短周期主族元素W、X、Y、Z的原子序数依次增大,Y和Z位于同一主族.m、n、p均为由这些元素组成的二元化合物,甲、乙、丙为其中三种元素对应的单质,丙为黄色固体,易溶在XZ2中,p是一种二元弱酸.上述物质的转化关系如图所示(反应条件省略).下列说法正确的是( )| A. | 原子半径:W<X<Y | |
| B. | W与X组成的化合物中可能含有极性键和非极性键 | |
| C. | Y与Z组成的化合物一定有漂白性 | |
| D. | W与X、Y、Z组成的简单化合物的稳定性:X>Y>Z |
分析 丙为黄色固体,应为S,易溶在XZ2中,可知X为C元素,Z为S元素,Y和Z位于同一主族,则Y为O元素,p是一种二元弱酸,且和n反应生成S单质,则p为H2S,由此可知W为H元素,结合转化关系可知乙为S,甲为O2,丙为H2,n为SO2,以此解答该题.
解答 解:由以上分析可知W为H、X为C、Y为O、Z为S元素,甲为O2,乙为S,丙为H2,m为H2O,n为SO2,p为H2S,
A.同周期元素从左到右原子半径逐渐减小,则C>O,故A错误;
B.H和C可形成多种烃,分子含有C-C键、C-H键,含有非极性键和极性键,故B正确;
C.如为SO3,则不具有漂白性,故C错误;
D.非金属性O>S>C,则对应的氢化物的稳定性性O>S>C,故D错误.
故选B.
点评 本题考查无机物的推断,为高频考点,侧重分析与推断能力的考查,注意元素化合物知识的应用,丙为推断的突破口,题目难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
16.四联苯 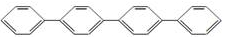 的一氯代物有( )
的一氯代物有( )
 的一氯代物有( )
的一氯代物有( )| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
17.一定条件下,在体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3mol Z,下列说法正确的是( )
| A. | 若增大压强,则物质Y的转化率减小 | |
| B. | 将容器体积变为5 L,Z的平衡浓度变为原来的2倍 | |
| C. | Y浓度变化表示的反应速率为0.0005 mol/(L•s ) | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H>0 |
14.某有机物M的结构简式为CH3CH=CHCH2COOH,下列有关说法正确的是( )
| A. | 能与乙醇发生酯化反应 | |
| B. | 能使酸性高锰酸钾溶液褪色 | |
| C. | 能与溴的四氯化碳溶液发生取代反应 | |
| D. | 1molM与足量Na完全反应能生成1molH2 |
11.下列有关苯的性质说法的是( )
| A. | 苯能使溴水褪色是因为苯与溴水发生了化学反应 | |
| B. | 欲从碘的苯溶液中分离出碘,通常采用萃取法 | |
| C. | 苯和不溶于水且密度比水大的四氯化碳都是无色液体,用试管和水就可以区别它们 | |
| D. | 因为苯通常是无色液体,所以在0℃的环境中可以直接将苯从试剂瓶倒人试管中 |
3.硫化钠(Na2S)在工业上用途广泛.某课题组用无水Na2SO4制备硫化钠的流程如下:
①取一定量的无水Na2SO4和碳粉进行隔绝空气高温灼烧;
②将灼烧产物冷却后,加入NaOH溶液进行碱浸
③过滤,滤液经过一系列的操作步骤后得到硫化钠晶体.
(1)过滤需要用到的主要玻璃仪器是漏斗、烧杯、玻璃棒.
(2)若灼烧所得气体为等物质的量的CO和CO2,写出灼烧时发生的化学反应方程为3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑.
(3)上述流程中采用a浸洗更好.
a.稀NaOH溶液b.热水c.氨水d.乙醇
(4)固体产物Na2S晶体中可能含有杂质,该课题组对固体产物的杂质成分提出以下假设:
假设一:杂质成分为NaOH;
假设二:杂质成分为Na2SO4;
假设三:杂质成分为NaOH和Na2SO4.
为验证假设三成立,课题组进行如下研究,请你完成下表中的内容:
:
①取一定量的无水Na2SO4和碳粉进行隔绝空气高温灼烧;
②将灼烧产物冷却后,加入NaOH溶液进行碱浸
③过滤,滤液经过一系列的操作步骤后得到硫化钠晶体.
(1)过滤需要用到的主要玻璃仪器是漏斗、烧杯、玻璃棒.
(2)若灼烧所得气体为等物质的量的CO和CO2,写出灼烧时发生的化学反应方程为3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑.
(3)上述流程中采用a浸洗更好.
a.稀NaOH溶液b.热水c.氨水d.乙醇
(4)固体产物Na2S晶体中可能含有杂质,该课题组对固体产物的杂质成分提出以下假设:
假设一:杂质成分为NaOH;
假设二:杂质成分为Na2SO4;
假设三:杂质成分为NaOH和Na2SO4.
为验证假设三成立,课题组进行如下研究,请你完成下表中的内容:
| 实验步骤 | 预期的实验现象和结论 |
| 步骤:取一定量的固体产物于试管中,加入适量蒸馏水进行溶解,然后往试管中加入适量的 CuCl2溶液并过滤. | \ |
| 步骤2: 取1的滤液加入酚酞试液,若溶液变红, | 说明有NaOH |
| 步骤3: 取1的滤液加入BaCl2溶液,若产生白色沉淀, | 说明有Na2SO4 |
20.某工业废水中仅含表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L.
甲同学欲探究废水的组成,进行了如下实验:
I.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量溶液,加入KSCN溶液无明显变化.
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由I、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
(3)将Ⅲ中红棕色气体(标况下)收集一满试管然后倒扣入水中(假设溶质不扩散),所得溶液的物质的量浓度为0.045mol/L(精确到千分位).
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Cu2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体为CuO和Fe2O3质量为1.6g.
| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl- CO32- NO3- SO42- SiO32- |
I.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量溶液,加入KSCN溶液无明显变化.
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由I、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
(3)将Ⅲ中红棕色气体(标况下)收集一满试管然后倒扣入水中(假设溶质不扩散),所得溶液的物质的量浓度为0.045mol/L(精确到千分位).
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Cu2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体为CuO和Fe2O3质量为1.6g.
 .
.