题目内容
14.下列叙述中,正确的是( )| A. | 铜和FeCl3溶液均能导电,但二者都不是电解质 | |
| B. | 分解反应的生成物中一定有单质 | |
| C. | 分散质粒子的直径在1×10-9~1×10-7cm之间的分散系属于胶体 | |
| D. | 氯气不能使干燥的有色布条褪色,液氯能使干燥的有色布条褪色 |
分析 A.电解质指:水溶液中或熔融状态下能够导电的化合物,导电必须是化合物自身电离出自由移动的离子;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质;
B.分解反应生成的产物不一定有单质生成;
C.胶体区别于其它分散系的本质特征是胶体粒子直径在1-100nm(10-7~10-9m)之间;
D.氯气不具有漂白性,氯气和水反应生成的次氯酸具有漂白性;
解答 解:A.铜是单质不是化合物,既不是电解质也不是非电解质,FeCl3溶液是混合物,是电解质溶液,均能导电,但二者都不是电解质,故A正确;
B.分解反应如CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,成物中无单质生成,故B错误;
C.分散质粒子的直径在1×10-9~1×10-7m之间的分散系属于胶体,故C错误;
D.氯气不具有漂白性,不能使干燥的有色布条褪色,液氯也不能使干燥的有色布条褪色,是氯气和水反应生成的次氯酸具有漂白性,故D错误;
故选A.
点评 本题考查了物质分类、物质组成、物质性质\物质变化等,主要是分散系组成和本质区别、氯气性质等,注意知识积累,题目难度不大.

练习册系列答案
相关题目
2.运用科学发展观,创建和谐社会,保护生存环境是每个公民的责任和义务.下列行为不符合社会发展与自然环境之间和谐的是( )
| A. | 推广垃圾分类投放、分类回收、分类处理 | |
| B. | 氮、磷的植物的营养元素,含氮、磷化合物的生活污水直接排放 | |
| C. | 使用沼气、太阳能、风能等能源代替传统的煤炭 | |
| D. | 研制开发燃料电池汽车,减少机动车尾气污染 |

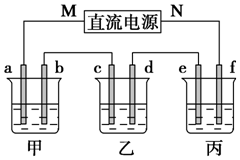 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极. 用DNA制造出一种臂长只有7nm的纳米级镊子,这种镊子能钳起分子或原子,并对它们随意组合。下列分散系中分散质的微粒直径与纳米级镊子具有相同数量级的是 ( )
用DNA制造出一种臂长只有7nm的纳米级镊子,这种镊子能钳起分子或原子,并对它们随意组合。下列分散系中分散质的微粒直径与纳米级镊子具有相同数量级的是 ( )