题目内容
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol可知,若将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ |
| C、由C(石墨)═C(金刚石)△H=+1.90 kJ?mol-1可知,金刚石比石墨稳定 |
| D、500℃、30MPa下,将0.5molN2(g)和1.5mol H2(g)置于密闭容器中充分反应生成0.2molNH3(g),放热9.3kJ,其热化学方程式为: N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ/mol |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、对于放热反应来说,反应物能量越高,反应放热越多;
B、醋酸是弱酸,没有完全电离,醋酸电离时吸热;
C、物质的能量越低越稳定;
D、合成氨是可逆反应,其焓变应据生成0.2mol氨气时放热多少计算.
B、醋酸是弱酸,没有完全电离,醋酸电离时吸热;
C、物质的能量越低越稳定;
D、合成氨是可逆反应,其焓变应据生成0.2mol氨气时放热多少计算.
解答:
解:A、对于放热反应来说,反应物能量越高,反应放热越多,等物质的量时,硫蒸汽比硫固体所含能量高,故A错误;
B、醋酸是弱酸,在水溶液中没有完全电离,醋酸电离时吸热,所以1mol醋酸与1mol氢氧化钠溶液反应放热少于强酸,故B正确;
C、石墨能量比金刚石低,物质的能量越低越稳定,故C错误;
D、0.2molNH3(g),放热9.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-93kJ/mol,故D错误;
故选B.
B、醋酸是弱酸,在水溶液中没有完全电离,醋酸电离时吸热,所以1mol醋酸与1mol氢氧化钠溶液反应放热少于强酸,故B正确;
C、石墨能量比金刚石低,物质的能量越低越稳定,故C错误;
D、0.2molNH3(g),放热9.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-93kJ/mol,故D错误;
故选B.
点评:本题考查了焓变的计算、中和热、物质的能量越低越稳定、可逆反应的焓变,题目难度中等.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
以下反应最符合绿色化学原子经济性(即:原子利用率为100%)要求的是( )
| A、甲苯与硝酸制TNT |
| B、乙烯聚合为聚乙烯高分子材料 |
| C、溴乙烷水解制乙醇 |
| D、甲烷与氯气制备一氯甲烷 |
“绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对环境的负作用.下列化学反应,不符合绿色化学概念的是( )
| A、消除硫酸厂尾气排放的SO2:SO2+2NH3+H2O=(NH4)2SO3 |
| B、消除制硝酸工业尾气的氮氧化物污染:NO2+NO+NaOH=2NaNO2+H2O |
| C、制CuSO4:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O |
| D、制Cu(NO3)2:3Cu+8HNO3(稀)=3 Cu(NO3)2+2NO↑+4H2O |
下列关于醇与酚的比较中正确的是( )
| A、醇和酚不能是同分异构体 |
| B、醇、酚的水溶液都能使石蕊试纸变红 |
| C、醇和酚都能与钠发生反应,放出氢气 |
| D、醇和酚都能与氢氧化钠溶液反应 |
X、Y是周期表中前20号中两种元素(非稀有气体元素),X原子的半径比Y的半径小,且具有相同的电子层数,下列有关叙述正确的是(选项中m、n均为正整数)( )
| A、若Y最高价为+5,则X最高价一定为+6或+7 |
| B、若Y元素形成的单质是气体,则X元素形成的单质一定也是气体 |
| C、若HnXOm为强酸,则X的氢化物溶液于水一定显酸性 |
| D、X的离子半径一定比Y离子半径小 |
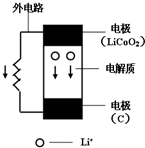 某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向).充电、放电时总反应可表示为:Li1-xCoO2+LixC6
某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向).充电、放电时总反应可表示为:Li1-xCoO2+LixC6| 充电 |
| 放电 |
| A、外电路上的“→”表示放电时的电流方向 |
| B、充电时阴极电极反应:LixC6-xe-═6C+xLi+ |
| C、放电时负极电极反应:LiCoO2-xe-═Li1-xCoO2+xLi+ |
| D、外电路有0.1mol e-通过,发生迁移的Li+的质量为0.7g |
下列关于乙醇的说法中,正确的是( )
| A、分子中含有C=O键 |
| B、官能团为羧基 |
| C、能使紫色石蕊试液变红 |
| D、可用碳酸钠溶液来鉴别乙醇和乙酸溶液 |
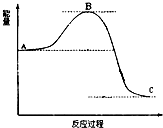 已知2SO2(g)+O2(g)
已知2SO2(g)+O2(g)