题目内容
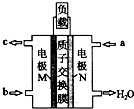 甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇 燃料电池的总反应式2CH40+302=2C02↑+4H20,如图是该燃料电池的示意图.下列说法错误的是( )
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇 燃料电池的总反应式2CH40+302=2C02↑+4H20,如图是该燃料电池的示意图.下列说法错误的是( )| A、燃料电池将化学能转化为电能 |
| B、a是甲醇,b是氧气 |
| C、质子从M电极区穿过交换膜移向N电极区 |
| D、负极反应:CH40-6e-+H20=C02↑+6H+ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、电池是化学能转化为电能;
B、据电池中存在质子交换膜可知,正极上氧气与氢离子结合生成水;
C、据电池中存在质子交换膜可知,正极上氧气与氢离子结合生成水,N电极区为正极,质子移向N极;
D、负极是甲醇反应,生成二氧化碳和氢离子.
B、据电池中存在质子交换膜可知,正极上氧气与氢离子结合生成水;
C、据电池中存在质子交换膜可知,正极上氧气与氢离子结合生成水,N电极区为正极,质子移向N极;
D、负极是甲醇反应,生成二氧化碳和氢离子.
解答:
解:从图上分析,电池中存在质子交换膜可知,电解液为酸性,氢离子在正极与氧气几乎生成水,正极反应式为:02+4H++4e-=H20,N为正极区,负极反应式为CH40-6e-+H20=C02↑+6H+,M为负极区,
A、电池是将化学能转化为电能的装置,故A正确;
B、a是氧气,b是甲醇,故B错误;
C、N为正极区,M为负极区,氢离子从负极移向正极,故C正确;
D、负极反应式为CH40-6e-+H20=C02↑+6H+,M为负极区,故D正确;
故选B.
A、电池是将化学能转化为电能的装置,故A正确;
B、a是氧气,b是甲醇,故B错误;
C、N为正极区,M为负极区,氢离子从负极移向正极,故C正确;
D、负极反应式为CH40-6e-+H20=C02↑+6H+,M为负极区,故D正确;
故选B.
点评:本题考查了燃料电池的电极反应和电解判断,据电池中存在质子交换膜和N极区生成水判断电极是解答本题的关键.

练习册系列答案
相关题目
用下列实验装置进行相应实验,能达到实验目的是-玻璃棒( )
A、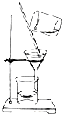 用如图所示装置除去Fe(OH)3胶体中含有的少量FeCl3杂质 |
B、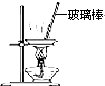 用如图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
C、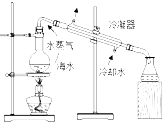 用如图所示装置从海水制取蒸馏水 |
D、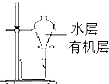 用如图所示装置分离酒精萃取碘水中的碘 |
一定温度下,满足下列条件的溶液一定呈酸性的是( )
| A、c(H+)>c(OH-)的任意水溶液 |
| B、加酚酞后显无色的溶液 |
| C、pH=6的某溶液 |
| D、能与金属Al反应放出H2的溶液 |
升高温度,下列数据不一定增大的是( )
| A、电离平衡常数Ka |
| B、水解平衡常数Kb |
| C、化学平衡常数K |
| D、水的离子积常数Kw |
下列关于金属钠的叙述中正确的是( )
| A、钠可以保存在煤油或四氯化碳中 |
| B、钠长久露置在空气中最终生成NaHCO3 |
| C、钠在空气中燃烧,火焰黄色,生成淡黄色的Na2O2 |
| D、钠与水反应的实验现象可以说明钠硬度小、熔点低、密度小于水 |
 A和甲是自石油和煤的两种基本化工原料,A是气态烃,甲是液态烃.B和D是生活中两种常见的有机物,F是高分子化合物.相互转化关系如图所示(已知:R-CHO
A和甲是自石油和煤的两种基本化工原料,A是气态烃,甲是液态烃.B和D是生活中两种常见的有机物,F是高分子化合物.相互转化关系如图所示(已知:R-CHO 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图.请回答: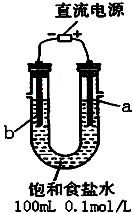 某化学研究小组用如图装置模拟步骤Ⅰ电解食盐水(用铁和石墨做电极材料).
某化学研究小组用如图装置模拟步骤Ⅰ电解食盐水(用铁和石墨做电极材料).