题目内容
相同物质的量浓度的下列化合物的水溶液,按pH减小顺序排列提( )
分析:根据盐的水解知识来确定醋酸钠和氯化铵的酸碱性,硫酸氢钠是一种能完全电离出H+的盐、NaNO3是一种中性盐来分析.
解答:解:硫酸氢钠是一种显强酸性的盐,氯化铵水解显示酸性,相同物质的量浓度,硫酸氢钠PH值比氯化铵小,NaNO3是一种中性盐,CH2COONa水解显碱性,
故pH减小顺序为:CH2COONa、NaNO3、NH4Cl、NaHSO4,
故选C.
故pH减小顺序为:CH2COONa、NaNO3、NH4Cl、NaHSO4,
故选C.
点评:本题主要考查学生盐的水解知识以及溶液的PH值和酸碱性之间的关系.

练习册系列答案
相关题目
已知同温度、同物质的量浓度的NaX溶液的pH值大于NaY溶液的pH值,据此,下列对两种对应酸(HX和HY)在相同温度和浓度下的比较中正确的是( )
| A、c(X-)>c(Y-) | B、电离程度:HX>HY | C、HY溶液的pH值>HX溶液的pH | D、HY溶液中的c(H+)>HX溶液中的c(H+) |
中学化学教材中有大量数据,下列为某同学对数据的利用情况,其中不正确的是( )
| A、用沸点数据推测两种液体混合物用蒸馏方法分离开来的可能性 | B、用几种一元弱酸的电离常数Ka来比较相同温度下相同物质的量浓度的这几种一元弱酸的钠盐溶液的碱性强弱 | C、用几种相同类型的难溶电解质的Ksp来比较相同温度下它们的溶解度的大小 | D、用熔、沸点数据来分析分子的稳定性 |
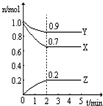
 2Z
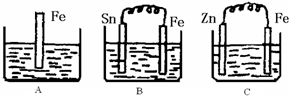
2Z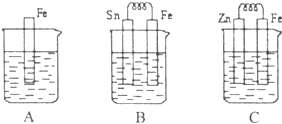 I.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.
I.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.