题目内容
从如图所示的某气体反应的能量变化分析,以下判断错误的是( )


| A、这是一个放热反应 |
| B、该反应可能需要加热 |
| C、生成物从气态变成液态时会放出热量 |
| D、生成物具有的总能量高于反应物具有的总能量 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、分析图象可知反应物能量高于生成物;
B、反应进行需要变化为活化分子可能需要吸收能量;
C、任何物质从气态变为液态时都会放热;
D、依据图象分析;
B、反应进行需要变化为活化分子可能需要吸收能量;
C、任何物质从气态变为液态时都会放热;
D、依据图象分析;
解答:
解:A、图象分析可知反应物能量高于生成物,反应是放热反应,故A正确;
B、反应可能需要吸收能量引发反应进行,故B正确
C、任何物质从气态变为液态时都会放热,故C正确;
D、从图上可见,反应物具有的能量高于生成物,故D错误;
故选D.
B、反应可能需要吸收能量引发反应进行,故B正确
C、任何物质从气态变为液态时都会放热,故C正确;
D、从图上可见,反应物具有的能量高于生成物,故D错误;
故选D.
点评:本题考查了物质能量变化的分析判断,图象分析是解题关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
将3.6g铁铜混合粉末,投入100mL c mol/L的稀硝酸中,金属粉末与硝酸恰好完全反应(还原产物只有NO),向反应后的溶液中加入足量的NaOH溶液,充分反应后将沉淀过滤、洗涤、灼烧至恒重后称量为4.8g.则c值不可能为( )
| A、1.2 | B、1.75 |
| C、2.0 | D、2.4 |
下列认识中不正确的是( )
| A、元素化学性质主要是由原子最外层电子数决定 |
| B、H、Ca、Mg、I 等元素都是短周期元素的 |
| C、元素原子的电子层数等于所在周期的周期序数 |
| D、主族元素原子的最外层电子数等于其所在族的族序数 |
下列反应的离子方程式正确的是( )
| A、碳酸镁溶于硫酸溶液 MgCO3+2H+═Mg2++H2O+CO2↑ |
| B、澄清的石灰水跟稀硝酸反应 Ca(OH)2+2H+=Ca2++2H2O |
| C、氧化钠与稀H2SO4混合 O2-+2H+=H2O |
| D、碳酸钙溶于醋酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
下列说法正确的是( )
| A、绿色食品就是颜色为绿色的食品 |
| B、有机食品就是只含有机物的食品 |
| C、维生素C广泛存在于新鲜水果和绿色蔬菜中 |
| D、食盐加碘是在食盐中加KIO3 |
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH固体已潮解 |
| B、向容量瓶加水时,液面低于刻度线即摇匀 |
| C、定容时不小心加水超过了刻度线,用胶头滴管直接吸出多余部分 |
| D、有少量NaOH溶液残留在烧杯内 |
下列离子方程式的书写中,正确的是( )
| A、碳酸氢钙溶液中加入足量烧碱溶液:Ca(HCO3)2+2OH-=CaCO3↓+CO32-+2H2O |
| B、向溴水中通入SO2:Br2+2H2O+SO2=4H++SO42-+2Br- |
| C、向氨水中通过量CO2:2NH3+H2O+CO2=2NH4++CO32-+H2O |
| D、向次氯酸钙溶液中通过少量的SO2:Ca2++2ClO-+SO2=CaSO3↓+2HClO |
1mol有机物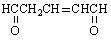 与足量氢气和新制氢氧化铜反应,消耗的氢气与氢氧化铜的量分别为( )
与足量氢气和新制氢氧化铜反应,消耗的氢气与氢氧化铜的量分别为( )
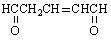 与足量氢气和新制氢氧化铜反应,消耗的氢气与氢氧化铜的量分别为( )
与足量氢气和新制氢氧化铜反应,消耗的氢气与氢氧化铜的量分别为( )| A、1mol 2mol |
| B、3mol 4mol |
| C、3mol 2mol |
| D、1mol 4mol |
