题目内容
11.已知在CH4中,C-H键间的键角为109°28′,NH3中N-H键间的键角为107°.H2O中O-H键间的键角为105°,则下列说法中正确的是( )| A. | 孤电子对与成键电子对间的斥力大于成键电子对间的斥力 | |
| B. | 孤电子对与成键电子对间的斥力小于成键电子对间的斥力 | |
| C. | 孤电子对与成键电子对间的斥力等于成键电子对与成键电子对间的斥力 | |
| D. | 题干中的数据不能说明孤电子对与成键电子对间的斥力与成键电子对与成键电子对间的斥力之间的大小关系 |
分析 CH4的中心原子没有孤电子对,其键角为109°28′,NH3的中心原子含有1个孤电子对,键角为107°,H2O的中心原子含有2个孤电子对,O-H键间的键角为105°,
孤对电子对成键电子的排斥作用较强.
解答 解:已知:CH4的中心原子没有孤电子对,其键角为109°28′,NH3的中心原子含有1个孤电子对,键角为107°,H2O的中心原子含有2个孤电子对,O-H键间的键角为105°,所以孤对电子对成键电子的排斥作用较强,即孤电子对与成键电子对间的斥力大于成键电子对间的斥力,故A正确.
故选A.
点评 本题考查了键角、分子的空间构型,题目难度不大,明确孤对电子对成键电子的排斥作用较强是解题的关键,注意把握题目中所给的信息.

练习册系列答案
相关题目
2.根据如图海水综合利用的工业流程图,判断下列说法正确的是.( )
已知:MgCl2.6H2O受热生成Mg(OH) Cl和HC1气体等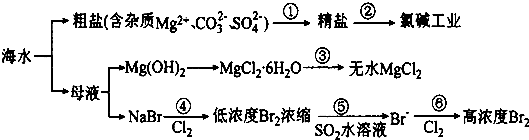
已知:MgCl2.6H2O受热生成Mg(OH) Cl和HC1气体等

| A. | 过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 | |
| B. | 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br一需消耗2.24LCl2 | |
| D. | 在过程③中将MgCl2.6H2O灼烧即可制得无水MgCl2 |
19.下列说法正确的是( )
| A. | 对于二元酸H2X,若NaHX溶液呈酸性,则H2X为强酸 | |
| B. | 升高温度,Na2A溶液的pH增大,H2A为弱酸 | |
| C. | 向烧碱溶液中通人CO2,一定存在c(Na+)=c(CO32-)+c(HCO3-)+c(H2C03) | |
| D. | 常温下,稀释氢氟酸溶液,$\frac{c({F}^{-})}{c(HF)•c(O{H}^{-})}$增大 |
6. 如图所示的装置常用于制取气体并检验气体的性质.下列有关说法正确的是( )
如图所示的装置常用于制取气体并检验气体的性质.下列有关说法正确的是( )
 如图所示的装置常用于制取气体并检验气体的性质.下列有关说法正确的是( )
如图所示的装置常用于制取气体并检验气体的性质.下列有关说法正确的是( )| A. | 关闭分液漏斗的活塞.将干燥管末端放人水中,微热烧瓶,有气泡从水中冒出,停止加热后,燥管内有水柱形成,表明装置不漏气 | |
| B. | 若装置用于制取氯气并验证其具有漂白性,则A中所用试剂为稀盐酸,B中所用药品为KMnO4固体,C中为品红溶液 | |
| C. | 若装置用于制取SO2并验证其具有漂白性,则A中所用试剂为浓硫酸,B中所用药品为Na2SO3固体,C中为酸性KMnO4溶液 | |
| D. | 若实验时B中盛放固体NaOH,A中为浓氨水,C中为稀AgNO3溶液,则实验过程中,C试管中看不到明显的实验现象 |
2.在密闭容器中发生反应X(g)+2Y(g)?2Z(g),若开始时,只加入X、Y两种物质,达到平衡后,测得混合气体中反应物总物质的量与生成物的物质的量相等,则X、Y的初始物质的量之比范围最准确的是( )
| A. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<$\frac{3}{2}$ | B. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<$\frac{1}{2}$ | C. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<4 | D. | $\frac{1}{2}$<$\frac{n(X)}{n(Y)}$<4 |