题目内容
17. 请按要求回答下列问题.
请按要求回答下列问题.(1)①打开K2,合并K1.A电极可观察到的现象是锌不断溶解;B极的电极反应式为Cu2++2e-═Cu.
②打开K1,合并K2.
A电极可观察到的现象是电极表面有红色固体附着;
B极的电极反应为Cu-2e-═Cu2+.
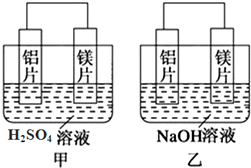
(2)判断原电池的正负极时,不仅要看金属活泼性顺序,还要注意此金属在电解质溶液中的活泼性.试回答下列问题:将铝片和铜片用导线连接,若插入浓硝酸中形成原电池,负极是铜片,若插入氢氧化钠溶液中形成原电池,负极是铝片.
分析 (1)①若打开K2,合并K1,形成原电池反应,Zn为负极,被氧化,Cu为正极,发生还原反应生成铜;
②若打开K1,合并K2,为电镀池,Cu为阳极,被氧化,Zn为阴极,发生还原反应生成铜;
(2)铝片和铜片插入浓HNO3溶液中,金属铝会钝化,金属铜和浓硝酸之间会发生自发的氧化还原反应;插入稀NaOH溶液中,金属铜和它不反应,金属铝能和氢氧化钠发生自发的氧化还原反应,在原电池中,自发氧化还原反应中的失电子的金属为负极,另一种金属或非金属是正极.
解答 解:(1)①若打开K2,合并K1,形成原电池反应,Zn为负极,被氧化而锌不断溶解,Cu为正极,发生还原反应生成铜,电极方程式为Cu2++2e-═Cu,
故答案为:锌不断溶解;Cu2++2e-═Cu;
②若打开K1,合并K2,为电镀池,Cu为阳极,被氧化,发生Cu-2e-═Cu2+,Zn为阴极,发生还原反应,锌极镀上一层红色的铜,
故答案为:电极表面有红色固体附着;Cu-2e-═Cu2+;
(2)铝片和铜片插入浓HNO3溶液中,金属铝会钝化,金属铜和浓硝酸之间会发生自发的氧化还原反应,此时金属铜时负极,金属铝是正极,
插入稀NaOH溶液中,金属铜和它不反应,金属铝能和氢氧化钠发生自发的氧化还原反应,此时金属铝是负极,金属铜是正极,
故答案为:铜片;铝片.
点评 本题综合考查原电池和电解池知识,为高频考点,注意把握原电池、电解池的工作原理以及电极方程式的书写,在判断原电池正负极时注意电解质溶液的性质,难度中等.

练习册系列答案
相关题目
7.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 18 g D2O所含的电子数为10NA | |
| B. | 12 g金刚石中含C-C键数为4NA | |
| C. | 标况下11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯的混合气体共14 g,其原子数为3NA |
8.下列反应既是氧化还原反应,又是吸热反应的是( )
| A. | 铝片与稀H2SO4反应 | B. | 灼热的炭与CO2反应 | ||
| C. | 高温煅烧石灰石 | D. | 甲烷在O2中的燃烧反应 |
5.下列反应中水作还原剂的是( )
| A. | F2+H2O | B. | Cl2+H2O | C. | Na+H2O | D. | Na2O2+H2O |
12.原子利用率=期望产物的总质量与生成物的总质量之比,原子利用率越高对环境污染越小.在下列制备环氧乙烷的反应中,原子利用率最高的是( )
| A. |  $\stackrel{催化剂}{→}$ $\stackrel{催化剂}{→}$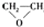 +HOCH2═O═CH2OH+2H2O +HOCH2═O═CH2OH+2H2O | B. | CH2═CH2+Cl2+Ca(OH)2? +CaCl2+H2O +CaCl2+H2O | ||
| C. | CH2═CH2+ (过氧乙酸)? (过氧乙酸)?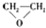 +C3HCOCH +C3HCOCH | D. | 2CH2═CH2+O2$\stackrel{催化剂}{→}$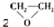 |
2.下列叙述错误的是( )
| A. | 油脂、淀粉、蔗糖和蛋白质在一定条件能发生水解反应 | |
| B. | 甲烷和苯都不能与溴水、酸性高锰酸钾溶液发生反应,但苯不属于饱和烃 | |
| C. | 甲烷与氯气制备一氯甲烷符合绿色原子经济要求 | |
| D. | 乙烯聚合为聚乙烯高分子材料符合绿色原子经济要求 |
9.一种塑料抗氧化剂C可通过下列反应合成:
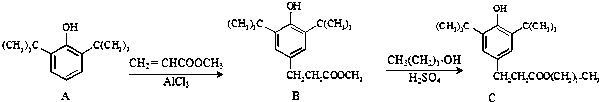
下列有关叙述正确的是( )

下列有关叙述正确的是( )
| A. | 物质A中所有碳原子有可能位于同一平面 | |
| B. | 物质B可与4molH2发生加成反应 | |
| C. | 用酸性KMnO4溶液鉴别抗氧化剂C中是否含有CH3(CH2)17OH | |
| D. | B生成C的反应类型为取代反应 |
6.有关元素X、Y、Z、D、E的信息如下:
请回答下列问题(用化学用语表示):
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)比较Y与Z的氢化物的稳定性HCl>H2S(用化学式表示).
(3)E元素与Y元素可形成EY2和EY3两种化合物,则下列说法中正确的是②③(填序号)
①通常实验室配制EY3溶液时,可直接用水溶解EY3固体
②EY2不能通过单质直接化合产生
③铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
④Y、Z、D的离子半径大小依次减小
(4)Y的最高价氧化物为无色液体,当0.25mol该物质与一定量的水混合得到一种稀溶液时,放出Q kJ的热量.写出该反应的热化学方程式Cl2O7(l)+H2O(l)═2HClO4(aq)△H=-4QkJ/mol.
(5)写出E在潮湿的空气中发生腐蚀时正极上的电极反应式O2+2H2O+4e-=4OH-.
| 元素 | 有关信息 |
| X | 元素主要化合价-2,原子半径为0.0074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 单质在X的单质中燃烧,产物是造成酸雨的罪魁祸首之一 |
| D | 最高价氧化物对应的水化物能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中的常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)比较Y与Z的氢化物的稳定性HCl>H2S(用化学式表示).
(3)E元素与Y元素可形成EY2和EY3两种化合物,则下列说法中正确的是②③(填序号)
①通常实验室配制EY3溶液时,可直接用水溶解EY3固体
②EY2不能通过单质直接化合产生
③铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
④Y、Z、D的离子半径大小依次减小
(4)Y的最高价氧化物为无色液体,当0.25mol该物质与一定量的水混合得到一种稀溶液时,放出Q kJ的热量.写出该反应的热化学方程式Cl2O7(l)+H2O(l)═2HClO4(aq)△H=-4QkJ/mol.
(5)写出E在潮湿的空气中发生腐蚀时正极上的电极反应式O2+2H2O+4e-=4OH-.