题目内容
9.A、B、C、D都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素,D原子的S电子与P电子数相等,E是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式回答下列问题: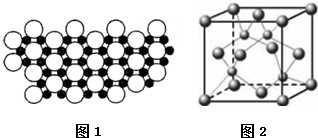
(1)A、B、C的第一电离能由小到大的顺序为C<O<N;D离子核外有10种运动状态的电子
(2)A的最高价氧化物对应的水化物分子中其中心原子采取sp2杂化
(3)已知A、C形成的化合物分子甲与B的单质分子结构相似,1mol甲中含有π键的数目为2NA(或1.204×1024)
(4)科学家发现硼化D在39K时呈超导性,在硼化D晶体的理想模型中,D原子和硼原子是分层排布的,一层D一层硼相间排列.图1是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是D原子投影,黑球是硼原子投影,图中的硼原子和D原子投影在同一平面上.根据图示确定硼化D的化学式为MgB2
(5)E的外围电子排布式是3d104s1;E的氢化物的晶体结构如图2所示,此氢化物化学式是CuH;写出此氢化物在氯气中燃烧的化学方程式2CuH+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl.
分析 A、B、C、D都是元素周期表中的短周期元素,它们的核电荷数依次增大,B原子的最外层p轨道的电子为半满结构,最外层电子排布为2s22p3,故B为N元素,第2周期元素A原子的核外成对电子数是未成对电子数的2倍,A的原子序数需要B,则A原子核外电子排布为1s22s22p2,为C元素;C是地壳中含量最高的元素,所以C是O元素;D原子的s电子与p电子数相等,其原子序数大于C,则其核外电子排布式为:1s22s22p63s2,故D为Mg元素;E是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满,故E元素原子各层电子数分别为2、8、18、1,为29号Cu元素,据此进行解答.
解答 解:A、B、C、D都是元素周期表中的短周期元素,它们的核电荷数依次增大,B原子的最外层p轨道的电子为半满结构,最外层电子排布为2s22p3,故B为N元素,第2周期元素A原子的核外成对电子数是未成对电子数的2倍,A的原子序数需要B,则A原子核外电子排布为1s22s22p2,为C元素;C是地壳中含量最高的元素,所以C是O元素;D原子的s电子与p电子数相等,其原子序数大于C,则其核外电子排布式为:1s22s22p63s2,故D为Mg元素;E是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满,故E元素原子各层电子数分别为2、8、18、1,为29号Cu元素,
(1)A、B、C为同一周期元素,同一周期元素的第一电离能随着原子序数的增大呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素,所以这三种元素的第一电离能从小到大顺序是C<O<N;D为Mg元素,其稳定离子为镁离子,镁离子核外的电子总数为10,则镁离子核外含有10种运动状态的电子,
故答案为:C<O<N;10;
(2)A为C元素,其最高价氧化物对应水化物为H2CO3,H2CO3中C原子最外层电子数全部成键,没有孤电子对,成1个C=O双键,2个C-O单键,杂化轨道数目为3,采取sp2杂化,
故答案为:sp2;
(3)C、O形成的化合物分子甲与N的单质分子结构相似,1mol氮气分子中含有2molπ键,所以1mol甲中含有π键的数目为2NA(或1.204×1024),
故答案为:2NA(或1.204×1024);
(4)根据投影可知,1个B原子为3个Mg原子共用,故属于一个Mg原子的B原子为$\frac{1}{3}$;1个Mg原子为6个B原子共用,故用于一个B原子的Mg原子为$\frac{1}{6}$,由此可知Mg、B原子数之比为:$\frac{1}{6}$:$\frac{1}{3}$=1:2,故硼化镁的化学式为MgB2,
故答案为:MgB2;
(5)E为Cu元素,其原子核外电子排布式为:1s22s22p63s23p63d104s1,则其外围电子排布式为:3d104s1;
该晶胞中铜离子和氢离子个数比是1:1,所以其化学式为CuH,氯气有强氧化性,氢化亚铜有强还原性,氯气能把氢化亚铜氧化生成氯化铜和氯化氢,所以氢化亚铜在氯气中燃烧的方程式为:2CuH+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl,
故答案为:3d104s1; CuH; 2CuH+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl.
点评 本题考查了位置、结构与性质的关系、晶胞的计算,题目难度中等,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力,注意掌握晶胞计算的方法与技巧,明确元素周期表结合、元素周期律的内容.

 )中所含有的共价键数目为( )
)中所含有的共价键数目为( )| A. | NA | B. | 0.7NA | C. | 1.9NA | D. | 7NA |
| A. | CH3CH2CH3 | B. | CH3CH(CH3)2 | C. | C (CH3)4 | D. | CH3CH2 CH2CH3 |

(1)【SO2的制备】:用亚硫酸钠与浓硫酸反应制备SO2的装置如图1(夹持仪器省略).图中的装置错误的是C(填字母);D的作用是吸收二氧化硫尾气,防止污染空气.
(2)【探究SO2的性质】:根据SO2中S元素的化合价,预测并通过实验验证SO2的性质.实验可选用的实验药品有浓硫酸、Na2SO3固体、Na2S溶液、FeCl3溶液、品红溶液等.探究过程实验装置如图2.(夹持仪器省略)
①请完成下列表格.
| 药品 | 作用 | |
| A | FeCl3溶液 | 验证SO2的还原性 |
| B | Na2S溶液 | 验证二氧化硫的氧化性 |
| C | 品红溶液 | 验证二氧化硫的漂白性 |
③在上述装置中通入过量的SO2,为了验证A中发生了氧化还原反应,取A中溶液分成两份,并设计了如下实验:
方案一:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去;
方案二:往第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红.
上述方案不合理的是方案一,原因是过量的二氧化硫能溶于水,也能使高锰酸钾褪色.
(3)【SO2的用途】:二氧化硫通常作为保护剂添加到葡萄酒中,有杀菌、抗氧化、改善风味和增酸的作用,但吸入过量二氧化硫对人体有害.我国国家标准规定葡萄酒中SO2的最大使用量为0.25g•L-1.图3为该小组对葡萄酒中的SO2进行收集与测量的装置.
①冷凝管中水的进口为:a(填“a”或“b”)
②A中加入200.00ml葡萄酒和适量盐酸,加热使SO2全部逸出并与B中H2O2完全反应,其化学方程式为SO2+H2O2=H2SO4.
③除去B中过量的H2O2,然后用0.0600mol•L-1NaOH标准溶液进行滴定,滴定至终点时,消耗NaOH溶液20.00ml,该葡萄酒中SO2含量为:0.192g•L-1.
(1)汽车尾气中的CO、NOx采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体.反应化学方程式可表示为:2xCO+2NOx $\frac{\underline{\;催化剂\;}}{\;}$2xCO2+N2.
(2)工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质.某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程.
提供的装置:
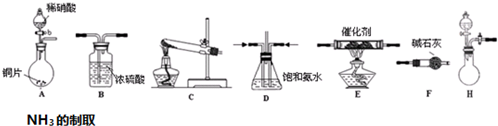
①所提供的装置中能快速、简便制取NH3的装置是:H(填仪器序号).
| 试剂组合序号 | 固体试剂(g) | NH3体积(mL) | |
| a | 12.0g Ca(OH)2 (过量) | 10.8g NH4Cl | 2688 |
| b | 10.8g (NH4)2SO4 | 2728 | |
| c | 12.0g NaOH (过量) | 10.8g NH4Cl | 3136 |
| d | 10.8g (NH4)2SO4 | 3118 | |
| e | 12.0g CaO (过量) | 10.8g NH4Cl | 3506 |
| f | 10.8g (NH4)2SO4 | 3584 | |
分析表中数据,实验室制NH3产率最高的是:f(填序号),其它组合NH3产率不高的原因是:因为用NH4Cl和NaOH或Ca(OH)2作反应物生成氨气的同时产生的水较多,则吸收溶解的NH3较多.
模拟尾气的处理
(3)选用上述部分装置,按下列顺序连接成模拟尾气处理装置:
①A中反应的离子方程式:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O.
②D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是:防止氨气溶解(或防止倒吸).
③D装置中的液体可换成c(填序号).
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
④该同学所设计的模拟尾气处理实验还存在的明显缺陷是:未反应的NO无法处理,会污染环境.
| A. | N2和H2 | B. | N2和H2O | C. | H2O | D. | N2 |
| A. | 按照有机物系统命名法,化合物的名称为:3,3-二乙基戊烷 | |
| B. | 分子式为C4H8O2的所有酯类的同分异构体共有6种 | |
| C. | 等物质的量的乙烯与碳酸二甲酯(CH3OCOOCH3)完全燃烧消耗氧气的量相同 | |
| D. | 丙烯酸(CH2=CHCOOH)和山梨酸(CH3CH=CHCH=CHCOOH)不是同系物,但它们与足量的氢气充分反应后的产物是同系物 |
| A. | 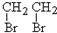 二溴乙烷 二溴乙烷 | B. | 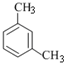 1,3-二甲苯 1,3-二甲苯 | ||
| C. |  2-乙基丁烷 2-乙基丁烷 | D. | CH2=CH-CH=CH2 1,3一二丁稀 |