题目内容
13.在一定条件下的恒容密闭容器中发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),图1表示反应过程中能量的变化,图2表示反应过程中物质浓度的变化
(1)该反应的焓变和熵变:△H<0,△S(熵变)<0,
(2)该反应的平衡常数K的表达式K=$\frac{c(C{H}_{3}OH)c({H}_{2}O)}{c(C{O}_{2}){c}^{3}({H}_{2})}$,温度降低,K的变化是增大
(3)升高温度,$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$的变化是(填变大,不变,减小)减小
(4)3分钟时氢气的反应速率是0.5mol/(L.min).
分析 (1)由图可知,反应物总能量大于生成物总能量,反应为放热反应,反应中气体的体积减小;
(2)K为生成物浓度幂之积与反应物浓度幂之积的比,该反应为放热反应,降低温度,平衡正向移动;
(3)升高温度,平衡逆向移动;
(4)结合v=$\frac{△c}{△t}$计算.
解答 解:(1)由图可知,反应物总能量大于生成物总能量,反应为放热反应,反应中气体的体积减小,则:△H<0,△S(熵变)<0,
故答案为:<;<;
(2)CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的K=$\frac{c(C{H}_{3}OH)c({H}_{2}O)}{c(C{O}_{2}){c}^{3}({H}_{2})}$,该反应为放热反应,降低温度,平衡正向移动,则K增大,
故答案为:K=$\frac{c(C{H}_{3}OH)c({H}_{2}O)}{c(C{O}_{2}){c}^{3}({H}_{2})}$;增大;
(3)升高温度,平衡逆向移动,则$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$减小,故答案为:减小;
(4)由图可知,3min内生成甲醇0.5mol/L,结合反应可知消耗氢气为1.5mol/L,则氢气表示的速率为$\frac{1.5mol/L}{3min}$=0.5mol/(L.min),
故答案为:0.5mol/(L.min).
点评 本题考查化学平衡常数及能量变化,为高频考点,把握图中能量变化、K的意义、速率计算及平衡移动为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
相关题目
1.中学化学涉及多种常数,下列说法正确的是( )
| A. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| B. | 某温度下,2L密闭容器中加入4mol A和2mol B发生反应: 3A(g)+2B(g)?4C(s)+2D(g).平衡时测得n(C)=1.6mol,反应的化学平衡常数表达式为K=$\frac{{c}^{4}(C){c}^{2}(D)}{{c}^{3}(A){c}^{2}(B)}$ | |
| C. | 温度一定时,当溶液中c(Ag+)•c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液 | |
| D. | 难溶电解质AB2饱和溶液中,c(A2+)=x mol•L-1,c(B-)=y mol•L-1,则Ksp值为4xy2 |
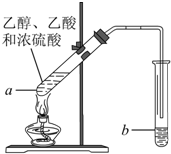 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.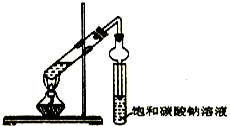 某同学用下列所示实验装置制取乙酸乙酯.回答以下问题:
某同学用下列所示实验装置制取乙酸乙酯.回答以下问题: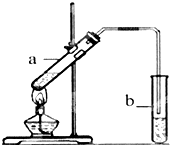 葡萄可用于酿酒.
葡萄可用于酿酒.