题目内容
18.下列关于元素周期表的描述正确的是( )| A. | 有7个周期,18个族 | |
| B. | 第IA族元素也称为碱金属元素 | |
| C. | 元素种类最多的族为第IIIB族 | |
| D. | 第七周期若排满,最多可排50种元素 |
分析 A、元素周期表有7横行被称为7个周期;元素周期表有18纵行被称为16个族;
B.IA族包含碱金属与氢元素;
C.元素周期表中第ⅢB族含有镧系和锕系;
D、第六、七周期均最多有32种元素.
解答 解:A、元素周期表有7横行被称为7个周期;元素周期表有18纵行被称为16个族,所以元素周期表有7个周期、16个族,故A错误;
B.IA族包含碱金属与氢元素,除氢之外的其它元素属于碱金属,故B错误;
C.元素周期表中第ⅢB族含有镧系和锕系,则第ⅢB族元素的种类最多,故C正确;
D、第六、七周期均最多有32种元素,不是50种,故D错误;
故选C.
点评 本题考查元素周期表的结构,为高频考点,比较基础,旨在考查学生对基础知识的掌握、有利于培养学生良好的科学素养.

练习册系列答案
相关题目
8.乙烯可通过石油裂解获得.下列有关乙烯性质的说法错误的是( )
| A. | 在常温常压下为气体 | B. | 不能发生氧化反应 | ||
| C. | 不能自身加成形成聚氯乙烯 | D. | 能使溴的CCl4溶液褪色 |
9.乙酸乙酯和丁酸互为同分异构体,下列方法中不能对二者进行鉴别的是( )
| A. | 利用金属钠 | B. | 利用质谱法 | ||
| C. | 利用红外光谱法 | D. | 利用核磁共振氢谱 |
6.设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
| A. | 标准状况下,22.4 LH2O中含有极性键的数目为2NA | |
| B. | 78 g Na2O2中含有的阴离子数为NA | |
| C. | 11 g重水(D218O)中含有的电子数力5NA | |
| D. | 常温常压下,5.6 g铁粉在7.1 g氯气中充分燃烧,转移的电子数为0.2NA |
3.氢化钠(NaH)是一种白色的离子化合物,其中钠元素是+1价;氢化钠与水反应放出H2.下列叙述中,正确的是( )
| A. | NaH在水中显碱性 | |
| B. | NaH中氢元素的离子的电子层排布与氖原子的电子层排布相同 | |
| C. | 微粒半径H-<Li+ | |
| D. | NaH与H2O反应时,水作还原剂 |
7.由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.
①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如下离子的溶液.
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象).阳极上发生的电极反应为2Cl--2e-=Cl2↑、4OH--4e-=2H2O+O2↑;阴极收集到的气体体积为(标准状况)6.72L.
①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如下离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/(mol•L-1) | 0.5 | 2 | 2 | 0.5 |
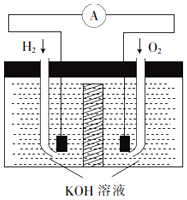 氢氧燃料电池是符合绿色化学理念的新型发电装置.其工作原理如图所示,该电池的电极表面镀了一层细小的铂粉,已知铂吸附气体的能力强,且性质稳定.
氢氧燃料电池是符合绿色化学理念的新型发电装置.其工作原理如图所示,该电池的电极表面镀了一层细小的铂粉,已知铂吸附气体的能力强,且性质稳定.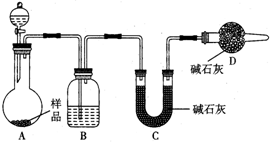 为测定放置已久的小苏打样品中纯碱的质量分数,设计如下实验方案:
为测定放置已久的小苏打样品中纯碱的质量分数,设计如下实验方案: