题目内容
(18分)为探究铁质材料与热浓硝酸的反应,某学习小组进行了以下实验:
[探究一]
(1)铁钉放在浓硫酸中浸泡后,再用蒸馏水冲洗,然后放入硫酸铜溶液中,铁钉表面无明显变化,其原因是_____________________。
(2)另称取铁钉6.0g放入15.0ml浓硝酸中,加热,充分应后得到溶液M并收集到气体N。为了探究溶液M中铁元素的价态,甲同学设计了如下实验:
有药品:
A.稀盐酸溶液
B.稀硫酸溶液
C.淀粉KI溶液
D.KMnO4溶液
E.NaOH溶液
F.H2O2溶液
G.KSCN溶液
仪器:试管和滴管
步骤1.取试样,滴加少量的______(填试剂字母),溶液的颜色变____色,则试样中含有Fe3+,发生反应的离子方程式为________________。
步骤2.再去适量的试样滴加少量的______(填试剂字母),若溶液_______,则试样中含有Fe2+。
[探究二]
乙同学设计以下装置探究气体N的成分。

(3)A装置的作用:______________________。
(4)B装置收集满气体后,通过气泡鼓入空气后,有红棕色气体生成,能否确定气体N中含NO____(填“能”或“不能”)?理由是________________。
(1)铁表面被钝化(2)G(或C)红(或蓝)Fe3++SCN-=Fe(SCN)3、2Fe3++2I-=I2+2Fe2+;
D;紫色褪去或变浅 (3)验证NO2的存在并除去NO
(4)不能;由于NO2溶于水也能生成硝酸和NO,故不能确定气体N中含有NO
【解析】
试题分析:(1)铁钉放入冷浓硫酸中,浓硫酸有较强的氧化性能使铁钉钝化阻止反应进一步进行,故答案为:铁表面被钝化;
(2)铁离子能与KSCN溶液反应显红色,另外铁离子还具有氧化性,能把碘化钾氧化生成单质碘,碘遇淀粉显蓝色,据此均可以检验铁离子,有关反应的离子方程式为Fe3++SCN-=Fe(SCN)3、2Fe3++2I-=I2+2Fe2+;亚铁离子具有还原性,能使酸性高锰酸钾溶液褪色,据此可以检验亚铁离子。
(3)铁与硝酸反应的还原产物是NO2或NO,由于NO2能干扰NO的检验,且NO2具有强氧化性,所以A装置中硫化钠的作用是验证NO2的存在并除去NO。
(4)由于NO2溶于水也能生成硝酸和NO,所以不能确定气体N中含有NO。
考点:考查铁与浓硫酸、浓硝酸反应的有关实验方案设计与探究

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案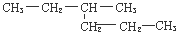 的命名正确的是
的命名正确的是