题目内容
实验室中拟用CuO、稀H2SO4、Fe三种物质为原料制取金属铜,试给出两种不同的制取方法,并比较其优劣,写出反应的化学方程式.
方法一: , .
方法二: , .
使用方法 更好,原因是 .
方法一:
方法二:
使用方法
考点:铜金属及其重要化合物的主要性质,制备实验方案的设计
专题:几种重要的金属及其化合物
分析:可以用活泼金属与铜盐溶液反应的方法获取铜,也可以用氢气还原氧化铜的方法获取铜,据此结合所给出的物质的性质、化学方程式的书写方法进行分析解答.
解答:
解:方法一:可以用氢气还原氧化铜的方法获取铜,要获得氢气可以使铁与硫酸反应的方法;铁与硫酸反应生成硫酸亚铁和氢气,氢气还原氧化铜生成铜和水,反应的化学方程式分别为:Fe+H2SO4═FeSO4+H2↑;H2+CuO
Cu+H2O;
可以用活泼金属与铜盐溶液反应的方法获取铜,铜盐溶液可以由氧化铜与硫酸反应生成;氧化铜与硫酸反应生成硫酸铜和水、铁和硫酸铜反应生成硫酸亚铁和铜,
反应的化学方程式分别为:CuO+H2SO4═CuSO4+H2O;CuSO4+Fe═FeSO4+Cu,综合两种方法可以发现:方法二更好,原因是方法一需要消耗大量的热量,且生成氢气不安全;
故答案为:方法一:用氢气还原氧化铜的方法获取铜;Fe+H2SO4═FeSO4+H2↑;H2+CuO
Cu+H2O;
方法二:用活泼金属与铜盐溶液反应的方法获取铜;CuO+H2SO4═CuSO4+H2O;CuSO4+Fe═FeSO4+Cu.
| ||
可以用活泼金属与铜盐溶液反应的方法获取铜,铜盐溶液可以由氧化铜与硫酸反应生成;氧化铜与硫酸反应生成硫酸铜和水、铁和硫酸铜反应生成硫酸亚铁和铜,
反应的化学方程式分别为:CuO+H2SO4═CuSO4+H2O;CuSO4+Fe═FeSO4+Cu,综合两种方法可以发现:方法二更好,原因是方法一需要消耗大量的热量,且生成氢气不安全;
故答案为:方法一:用氢气还原氧化铜的方法获取铜;Fe+H2SO4═FeSO4+H2↑;H2+CuO
| ||
方法二:用活泼金属与铜盐溶液反应的方法获取铜;CuO+H2SO4═CuSO4+H2O;CuSO4+Fe═FeSO4+Cu.
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述不正确的( )
| A、10g质量分数为46%的乙醇的水溶液中,氢原子的总数为0.6NA |
| B、5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA |
| C、50 mL 12 mol?L-1 浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| D、常温常压下,46g NO2与N2O4的混合气体中含有的原子总数为3NA |
在含有Fe3+、Fe2+、Al3+的稀溶液中加入足量Na2O2固体,充分作用后,再加入过量稀盐酸,完全反应,则离子数目没有变化的是( )
| A、Fe3+、Al3+ |
| B、Al3+ |
| C、Fe2+、 |
| D、Fe3+ |
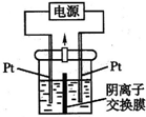 电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-=IO3-+5I-+3H2O.下列说法不正确的是( )
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-=IO3-+5I-+3H2O.下列说法不正确的是( )| A、右侧发生的电极方程式:2H2O+2e-=H2↑+2OH- | ||||
| B、电解结束时,右侧溶液中含有IO3- | ||||
C、电解槽内发生反应的总化学方程式KI+3H2O
| ||||
| D、如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变 |

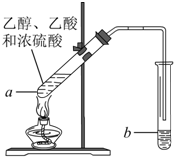 在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.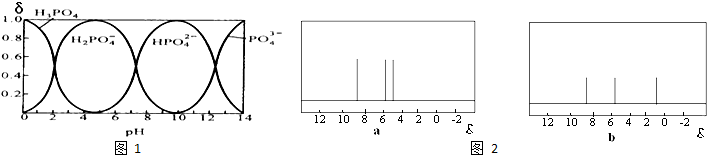
 某化学研究性学习小组在实验室整理化学试剂时,发现一个盛有无色溶液的试剂瓶的标签污损,如右图所示.同学们根据中学化学知识,对该试剂的成分进行了一系列猜想和探究.
某化学研究性学习小组在实验室整理化学试剂时,发现一个盛有无色溶液的试剂瓶的标签污损,如右图所示.同学们根据中学化学知识,对该试剂的成分进行了一系列猜想和探究.