题目内容
在101KPa、150℃条件下,0.1mol某烷烃充分燃烧后,将生成的气体通过盛有足量浓硫酸的洗气瓶,浓硫酸质量增重12.6g,然后再通过碱石灰,气体被完全吸收,碱石灰质量增加26.4g.请回答下列问题:
(1)写出该烷烃的分子式: ,该烷烃有 种同分异构体;
(2)若该烷烃的一氯代物有两种同分异构体,写出该烷烃的结构简式并命名: , .
(1)写出该烷烃的分子式:
(2)若该烷烃的一氯代物有两种同分异构体,写出该烷烃的结构简式并命名:
考点:有关有机物分子式确定的计算,同分异构现象和同分异构体
专题:
分析:浓硫酸质量增重12.6g,然后再通过碱石灰,气体被完全吸收,碱石灰质量增加26.4g,
浓硫酸增重12.6g为生成水的质量,碱石灰增重26.4g为燃烧生成二氧化碳的质量,
根据n=
计算水、二氧化碳的物质的量,
根据原子守恒确定有机物X分子中C、H原子数目及最简式、分子式,再根据该烷烃的同分异构体中等效氢原子数目确定满足条件的该烷烃的结构简式.
浓硫酸增重12.6g为生成水的质量,碱石灰增重26.4g为燃烧生成二氧化碳的质量,
根据n=
| m |
| M |
根据原子守恒确定有机物X分子中C、H原子数目及最简式、分子式,再根据该烷烃的同分异构体中等效氢原子数目确定满足条件的该烷烃的结构简式.
解答:
解:(1)浓硫酸增重12.6g为生成水的质量,则水的物质的量n(H2O)=
=0.7mol,n(H)=2n(H2O)=1.4mol,
碱石灰增重26.4g为燃烧生成二氧化碳的质量,二氧化碳的物质的量为:n(CO2)=
=0.6molmol,n(C)=n(CO2)=0.6mol,
X的分子中碳氢个数之比为:N(C):N(H)=0.6mol:1.4mol=6:14,由于X中H原子已经达到饱和,所以该有机物的分子式为C6H14;
烷烃C6H14的同分异构体为:①主链为6个C,不存在支链的为正己烷:CH3CH2CH2CH2CH2CH3;
②主链为5个C,侧链为1个甲基的同分异构体为有2种:CH3CH2CH2CH(CH3)CH3、CH3CH2CH(CH3)CH2CH3;
③主链为4个C,侧链不可能为乙基,只能为两个两个甲基,该同分异构体有3种:CH3CH(CH3)CH(CH3)CH3、CH3CH2C(CH3)2CH3;
④支链若为3个C,则侧链含有3个甲基或1个甲基1个乙基或者1个丙基,都不可能,所以己烷的主链最少4个C;
根据以上分析可知,己烷的同分异构体有:1+2+2=5,
故答案为:C6H14;5;
(2)该烷烃的一氯代物有2种同分异构体,说明己烷中含有2种等效氢原子,分子中含有2种等效H的己烷有CH3CH(CH3)CH(CH3)CH3,为2,3-二甲基丁烷;
故答案为:CH3CH(CH3)CH(CH3)CH3;2,3-二甲基丁烷.
| 12.6g |
| 18g/mol |
碱石灰增重26.4g为燃烧生成二氧化碳的质量,二氧化碳的物质的量为:n(CO2)=
| 26.4g |
| 44g/mol |
X的分子中碳氢个数之比为:N(C):N(H)=0.6mol:1.4mol=6:14,由于X中H原子已经达到饱和,所以该有机物的分子式为C6H14;
烷烃C6H14的同分异构体为:①主链为6个C,不存在支链的为正己烷:CH3CH2CH2CH2CH2CH3;
②主链为5个C,侧链为1个甲基的同分异构体为有2种:CH3CH2CH2CH(CH3)CH3、CH3CH2CH(CH3)CH2CH3;
③主链为4个C,侧链不可能为乙基,只能为两个两个甲基,该同分异构体有3种:CH3CH(CH3)CH(CH3)CH3、CH3CH2C(CH3)2CH3;
④支链若为3个C,则侧链含有3个甲基或1个甲基1个乙基或者1个丙基,都不可能,所以己烷的主链最少4个C;
根据以上分析可知,己烷的同分异构体有:1+2+2=5,
故答案为:C6H14;5;
(2)该烷烃的一氯代物有2种同分异构体,说明己烷中含有2种等效氢原子,分子中含有2种等效H的己烷有CH3CH(CH3)CH(CH3)CH3,为2,3-二甲基丁烷;
故答案为:CH3CH(CH3)CH(CH3)CH3;2,3-二甲基丁烷.
点评:本题考查了确定有机物分子式、结构简式的方法及同分异构体的书写,为高频考点,侧重于学生的分析、计算能力的考查,题目难度中等,注意掌握确定有机物分子式、结构简式的方法,(2)为本题的难点、易错点,注意掌握确定有机物分子中等效氢原子数目的方法.

练习册系列答案
相关题目
将1.12g铁粉加入到25mL2mol?L-1的氯化铁溶液中,充分反应后,其结果是( )
| A、铁有剩余 |
| B、反应中氧化产物与还原产物的质量之比为2:5 |
| C、往溶液滴入KSCN溶液显红色 |
| D、溶液中的Fe2+和Fe3+的物质的量之比为1:6 |
把x mol CO2通过足量的Na2O2后再与y mol NO混合,充分反应后测得剩余气体中没有氧气.若x与y之和为0.3mol,剩余气体为0.15mol(忽略N2O4的影响),则下列叙述中不正确的是( )
| A、x:y=1:1 |
| B、充分反应后,生成15.9 g Na2CO3 |
| C、充分反应后,生成0.25 mol Na2CO3 |
| D、生成氧气的过程中共转移电子0.15 mol |
下面是4种有机弱酸,强弱顺序为: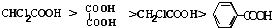 下列说法中不正确的是( )
下列说法中不正确的是( )
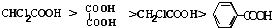 下列说法中不正确的是( )
下列说法中不正确的是( )A、等浓度等体积的4种酸中和碱的能力: |
B、等浓度的4种酸溶液中水电离出的c水(H+): >CH2ClCOOH> >CH2ClCOOH> >CHCl2COOH >CHCl2COOH |
C、反应 +2CH2ClCOO-→ +2CH2ClCOO-→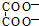 +2CH2ClCOOH一定能够发生 +2CH2ClCOOH一定能够发生 |
| D、由题中信息可推知酸性:CH2FCOOH>CH2ClCOOH |
 向100mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M.通入二氧化碳的体积V(标准状况下)与M的质量W的关系如图所示.请回答下列问题:
向100mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M.通入二氧化碳的体积V(标准状况下)与M的质量W的关系如图所示.请回答下列问题: