题目内容
18.下列分离或提纯有机物的方法正确的是( )| 选项 | 待提纯物质 | 杂质 | 除杂试剂及主要操作方法 |
| A | 乙烷 | 乙烯 | 酸性KMnO4溶液,洗气 |
| B | 溴苯 | 溴 | NaOH溶液,分液 |
| C | 乙酸 | 乙醇 | 金属钠,蒸馏 |
| D | 乙醇 | 水 | 生石灰,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙烯被高锰酸钾氧化生成二氧化碳气体;
B.溴与氢氧化钠溶液反应;
C.二者都与钠反应;
D.应用蒸馏的方法.
解答 解:A.乙烯被高锰酸钾氧化生成二氧化碳气体,引入新杂质,应用溴水除杂,故A错误;
B.溴与氢氧化钠溶液反应,而溴苯不反应,可加入氢氧化钠溶液除杂,故B正确;
C.二者都与钠反应,直接蒸馏,故C错误;
D.酒精与水的沸点不同,应用蒸馏的方法除杂,CaO与水反应放热,如过滤,易导致酒精挥发,故D错误.
故选B.
点评 本题考查物质的分离、提纯和除杂等问题,为高频考点,侧重考查学生的分析能力,题目难度不大,根据除杂是不能引入新的杂质、不能影响被提纯的物质的性质和量,并且操作简单可行,除杂时要结合物质的物理性质和化学性质进行分离.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
9.分子式为 C7H16的烷烃中,含有三个甲基的同分异构体共几种( )
| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 4 种 |
6.下列有机实验操作或叙述正确的是( )
| A. | 将乙烯和乙炔气体分别通入溴的四氯化碳溶液中,两者都褪色 | |
| B. | 甲烷和氯气在室温下的光照环境中可以稳定存在 | |
| C. | 苯能使溴水褪色是因为二者反应生成了溴苯 | |
| D. | 要除去乙烷中的乙烯制得纯净的乙烷,将混合气体通入酸性高锰酸钾溶液中 |
13.下列配制溶液的操作中,对溶液的浓度没影响的是( )
| A. | 称取碳酸钠晶体(Na2CO3•10H2O)100g来配制0.5mol/L的Na2CO3溶液1000mL | |
| B. | 配制NH3NO3溶液,在烧杯中溶解后立即注入容量瓶,并立即进行下面的各项操作 | |
| C. | 定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加入少量水至刻度线 | |
| D. | 容量瓶用蒸馏水洗净后未经干燥马上用来配制溶液 |
3.金属镓是一种广泛用于电子工业和通讯领域的重要金属,镓元素(31Ga)在元素周期表中位于第四周期,ⅢA族,化学性质与铝元素相似.
(1)工业上利用Ga与NH3合成固体半导体材料氮化镓(GaN)同时有氢气生成,反应中,生成3mol H2时放出30.8KJ的热.
①反应的热化学方程式是2Ga(s)+2NH3(g)?2GaN(s)+3H2(g)△H=-30.8KJ/mol.
②反应的化学平衡常数表达式是$\frac{{c}^{3}({H}_{2})}{{c}^{2}(N{H}_{3})}$;温度升高时,反应的平衡常数变小.(填“变大”“变小”或“不变”)
③在密闭体系内进行上述可逆反应,下列有关表达正确的是A.

A.图象Ⅰ中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压
B.图象Ⅱ中纵坐标可以为镓的转化率
C.图象Ⅲ中纵坐标可以为化学反应速率
D.图象Ⅳ中纵坐标可以为体系内混合气体平均相对分子质量
④氮化镓(GaN)性质稳定,但能缓慢的溶解在热的NaOH溶液中,该反应的离子方程式是GaN+OH-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$GaO2-+NH3↑.
(2)将一块镓铝合金完全溶于烧碱溶液中得到溶液X.已知:
往X溶液中缓缓通入CO2,最先析出的氢氧化物是Al(OH)3.
(3)工业上电解精炼镓的原理如下:待提纯的粗镓(内含Zn、Fe、Cu杂质)为阳极,高纯度镓为阴极,NaOH溶液为电解质溶液.在电流作用下使粗镓在阳极溶解进入电解质溶液,离子迁移到达阴极并在阴极放出电析出高纯镓.
①已知离子氧化性顺序为:Zn2+<Ga3+<Fe2+<Cu2+,电解精炼镓时阳极泥的成分是Fe、Cu.
②GaO2-在阴极放电的电极方程式是GaO2-+3e-+2H2O=Ga+4OH-.
(1)工业上利用Ga与NH3合成固体半导体材料氮化镓(GaN)同时有氢气生成,反应中,生成3mol H2时放出30.8KJ的热.
①反应的热化学方程式是2Ga(s)+2NH3(g)?2GaN(s)+3H2(g)△H=-30.8KJ/mol.
②反应的化学平衡常数表达式是$\frac{{c}^{3}({H}_{2})}{{c}^{2}(N{H}_{3})}$;温度升高时,反应的平衡常数变小.(填“变大”“变小”或“不变”)
③在密闭体系内进行上述可逆反应,下列有关表达正确的是A.

A.图象Ⅰ中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压
B.图象Ⅱ中纵坐标可以为镓的转化率
C.图象Ⅲ中纵坐标可以为化学反应速率
D.图象Ⅳ中纵坐标可以为体系内混合气体平均相对分子质量
④氮化镓(GaN)性质稳定,但能缓慢的溶解在热的NaOH溶液中,该反应的离子方程式是GaN+OH-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$GaO2-+NH3↑.
(2)将一块镓铝合金完全溶于烧碱溶液中得到溶液X.已知:
| Al(OH)3 | Ga(OH)3 | |
| 酸式电离常数Ka | 2×10-11 | 1×10-2 |
| 碱式电离常数Kb | 1.3×10-33 | 1.4×10-34 |
(3)工业上电解精炼镓的原理如下:待提纯的粗镓(内含Zn、Fe、Cu杂质)为阳极,高纯度镓为阴极,NaOH溶液为电解质溶液.在电流作用下使粗镓在阳极溶解进入电解质溶液,离子迁移到达阴极并在阴极放出电析出高纯镓.
①已知离子氧化性顺序为:Zn2+<Ga3+<Fe2+<Cu2+,电解精炼镓时阳极泥的成分是Fe、Cu.
②GaO2-在阴极放电的电极方程式是GaO2-+3e-+2H2O=Ga+4OH-.
10.下列环境相同时间内,钢铁能得到有效保护的是( )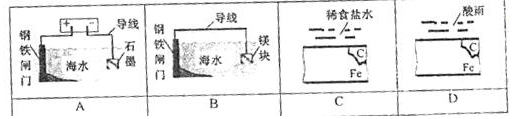

| A. | A | B. | B | C. | C | D. | D |
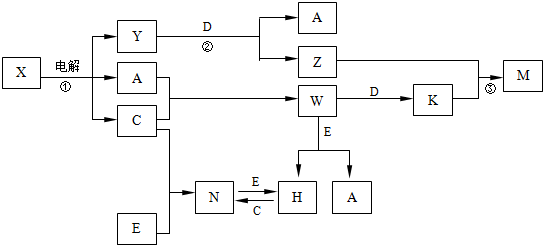
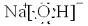 ,构成C单质的元素在周期表中位于第三周期第VIIA族
,构成C单质的元素在周期表中位于第三周期第VIIA族