题目内容
相同物质的量浓度的NaCN和NaClO溶液相比,前者的pH较大,则下列有关同温、同体积和同浓度的HCN和HClO叙述中,正确的是( )
| A、酸性:HCN>HClO |
| B、浓度:c(CN-)<c(ClO-) |
| C、pH:HClO>HCN |
| D、与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:根据盐的水解规律:越弱越水解,NaCN和NaClO溶液相比,前者的pH较大,可以得出酸性的强弱,酸性越强,电离程度越大,酸和氢氧化钠反应消耗氢氧化钠的量取决于酸的物质的量的多少.
解答:
解:A、NaCN和NaClO溶液相比,前者的pH较大,可以得出酸性HCN<HClO,故A错误;
B、同浓度的HCN和HClO,酸性HCN<HClO,所以次氯酸的电离程度大于氢氰酸,即c(CN-)<c(ClO-),故B正确;
C、酸性HCN<HClO,同体积和同浓度的HCN和HClO的pH大小顺序是:HClO<HCN,故C错误;
D、同体积和同浓度的HCN和HClO,其物质的量是相等的,与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO=HCN,故D错误.
故选B.
B、同浓度的HCN和HClO,酸性HCN<HClO,所以次氯酸的电离程度大于氢氰酸,即c(CN-)<c(ClO-),故B正确;
C、酸性HCN<HClO,同体积和同浓度的HCN和HClO的pH大小顺序是:HClO<HCN,故C错误;
D、同体积和同浓度的HCN和HClO,其物质的量是相等的,与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO=HCN,故D错误.
故选B.
点评:本题考查学生盐的水解原理和应用知识,注意知识的梳理和归纳是解题的关键,难度不大.

练习册系列答案
相关题目
下列能鉴别CO2和SO2的是 ( )
| A、品红溶液 |
| B、澄清石灰水 |
| C、紫色石蕊试液 |
| D、氯化钡溶液 |
能正确表示下列反应的离子方程式是( )
| A、在碳酸氢钠溶液中加入盐酸:HCO3-+H+=CO2↑+H2O |
| B、把金属铁放入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| C、向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- |
| D、钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
用铝热法还原下列化合物,制得金属各1mol,需消耗铝最少的是( )
| A、MnO2 |
| B、WO3 |
| C、Fe3O4 |
| D、Cr2O3 |
两种金属的混合物15g,溶于足量稀H2SO4,生成氢气0.5mol.则混合物不可能是( )
| A、Cu和Mg |
| B、Zn和Fe |
| C、Na和Al |
| D、Al和Fe |
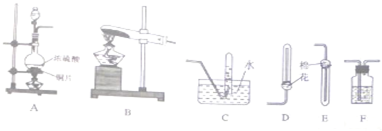
按如图所示装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )


| A、若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 |
| B、若A为醋酸,B为贝壳,C中盛澄清石灰水,则C中溶液无变化 |
| C、若A为浓氨水,B为生石灰,C中AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解 |
| D、实验仪器D主要起到防止溶液倒吸的作用 |