题目内容
19.从废液FeCl3、FeCl2、CuCl2中回收Cu,同学们设计了如下方案:废液中加入过量的铁粉,过滤,向铁、铜混合物中加入足量的盐酸,过滤后得到铜.上述过程中发生的所有反应的离子方程式为:2Fe3++Fe=3Fe2+,Fe+Cu2+=Cu+Fe2+,Fe+2H+=Fe2++H2↑这些反应所涉及的四种阳离子的氧化性顺序由大到小为Fe3+>Cu2+>H+>Fe2+.分析 整个过程中涉及废液中加入过量的铁粉,铁与氯化铁溶液和铁与氯化铜反应,铁与氢离子反应,反应的离子方程式为:2Fe3++Fe=3Fe2+,Fe+Cu2+=Cu+Fe2+,Fe+2H+=Fe2++H2↑;根据强制弱判断四种阳离子的氧化性,由此分析解答.
解答 解:涉及废液中加入过量的铁粉,铁与氯化铁溶液和铁与氯化铜反应,铁与氢离子反应,反应的离子方程式为:2Fe3++Fe=3Fe2+,Fe+Cu2+=Cu+Fe2+,Fe+2H+=Fe2++H2↑;根据强制弱得到:Fe3+>Cu2+>H+>Fe2+,故答案为:2Fe3++Fe=3Fe2+,Fe+Cu2+=Cu+Fe2+,Fe+2H+=Fe2++H2↑; Fe3+>Cu2+>H+>Fe2+.
点评 本题考查氧化还反应的相关知识和离子反应方程式的书写,学生根据强制弱来判断微粒氧化性的强弱,比较容易.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
10.在铜.锌与稀硫酸组成的原电池中,下列说法正确的是( )
| A. | 锌是负极,发生还原反应 | B. | 锌是负极,发生氧化反应 | ||
| C. | 铜是负极,发生还原反应 | D. | 铜是负极,发生氧化反应 |
8.下列变化过程中,只破坏离子键的是( )
| A. | 水变成冰 | B. | 电解熔融NaCl | C. | HCl溶于水 | D. | NH4Cl受热分解 |
4.下列关于糖类、蛋白质、油脂的说法正确的是( )
| A. | 糖类在一定条件下都可以水解生成乙醇和二氧化碳 | |
| B. | 乙酸乙酯和油脂都属于酯类物质,碱性条件水解称之为皂化反应 | |
| C. | 硝酸汞溶液加入到鸡蛋清中,可以使蛋清液盐析而沉淀下来 | |
| D. | 淀粉在稀硫酸加热催化下,水解产物葡萄糖的检出,先加入NaOH溶液后加入银氨溶液水浴加热,看是否有银镜出现.若出现银镜,证明有葡糖糖生成 |
 ,则该有机物核磁共振氢谱有3个峰.
,则该有机物核磁共振氢谱有3个峰.


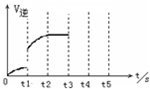 可逆反应Fe(s)+CO2(g)?FeO(s)+CO(g),在温度938K时,平衡常数K=1.47,在1173K时,K=2.15.
可逆反应Fe(s)+CO2(g)?FeO(s)+CO(g),在温度938K时,平衡常数K=1.47,在1173K时,K=2.15.