题目内容
对于下列事实的解释错误的是( )
| A、在蔗糖中加入浓硫酸后变黑,说明浓硫酸具有脱水性 |
| B、常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 |
| C、浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 |
| D、氨水可使酚酞试剂变为红色,说明氨水呈碱性 |
考点:浓硫酸的性质,氨的化学性质,硝酸的化学性质
专题:氧族元素,氮族元素
分析:A.在蔗糖中加入浓硫酸后变黑体现浓硫酸的脱水性;
B.常温下,浓硝酸和铝发生钝化现象;
C.光照条件下,浓硝酸分解;
D.无色酚酞试液遇碱变红色.
B.常温下,浓硝酸和铝发生钝化现象;
C.光照条件下,浓硝酸分解;
D.无色酚酞试液遇碱变红色.
解答:
解:A.浓硫酸能将蔗糖中的H、O以2:1水的形式脱去而体现脱水性,故A正确;
B.常温下,浓硝酸和铝发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,故B错误;
C.光照条件下,浓硝酸分解生成二氧化氮、氧气和水,二氧化氮溶于硝酸而使溶液呈黄色,故C正确;
D.氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而使溶液呈碱性,无色酚酞试液遇碱变红色,故D正确;
故选B.
B.常温下,浓硝酸和铝发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,故B错误;
C.光照条件下,浓硝酸分解生成二氧化氮、氧气和水,二氧化氮溶于硝酸而使溶液呈黄色,故C正确;
D.氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而使溶液呈碱性,无色酚酞试液遇碱变红色,故D正确;
故选B.
点评:本题考查了浓硫酸、浓硝酸、氨水的性质,知道浓硫酸的三大性质、浓硝酸的不稳定性等知识点即可解答,注意铝发生钝化时不是不反应,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某气体物质,经测定其蒸气密度折合成标准状况为1.63g/L.该化合物可能是下列的( )
| A、HCl |
| B、H2S |
| C、CH4 |
| D、C2H6 |
下列说法正确的是( )
| A、煤经气化、液化和干馏三个物理变化过程,可变为清洁能源 |
| B、油脂、淀粉、蔗糖和葡萄糖在一定条件都能发生水解反应 |
| C、棉花、羊毛、腈纶和涤纶都属于合成纤维 |
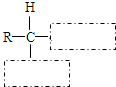
D、用甘氨酸(H2N-CH2-COOH)和丙氨酸( )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
结构简式是CH2=CHCH2CHO的物质不能发生( )
| A、加成反应 | B、还原反应 |
| C、酯化反应 | D、氧化反应 |
下列叙述正确的是( )
| A、离子键只存在于金属阳离子与酸根阴离子之间 |
| B、两种非金属元素形成AB型化合物,它一定含共价键 |
| C、物质中化学键破坏了,一定发生化学变化 |
| D、化学键类型一定由元素类别决定 |
氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是( )
| A、1mol/L甲酸溶液的pH约为3 |
| B、HCN中滴入石蕊试液,溶液显示为红色 |
| C、10mL 1mol/L HCN恰好与10 mL 1mol/L NaOH溶液完全反应 |
| D、用HCN溶液做导电性实验,灯泡很暗 |
下列说法正确的是( )
A、四氯化碳分子的电子式为: |
| B、只用一种试剂就能鉴别:苯、四氯化碳、己烯 |
| C、乙烯的结构简式:CH2CH2 |
| D、下列物质沸点由高到低的是:戊烷;新戊烷;2-甲基丁烷;丁烷;丙烷 |
 :
: