题目内容
2.下列装置用于实验室制氨气或验证氨气的某化学性质,其中能达到实验目的是( )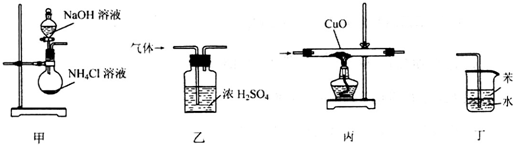
| A. | 用装置甲制取氨气 | B. | 用装置乙除去氨气中的水蒸气 | ||
| C. | 用装置丙验证氨气具有还原性 | D. | 用装置丁吸收尾气 |
分析 A.不加热生成一水合氨;
B.氨气与硫酸反应;
C.氨气与CuO反应生成氮气、Cu和水;
D.苯的密度比水的密度小,在上层,不能隔绝气体与水.
解答 解:A.不加热生成一水合氨,图中缺少酒精灯加热制备氨气,故A错误;
B.氨气与硫酸反应,则不能干燥氨气,故B错误;
C.氨气与CuO反应生成氮气、Cu和水,N元素的化合价升高,则氨气具有还原性,故C正确;
D.苯的密度比水的密度小,在上层,不能隔绝气体与水,则图中装置不能吸收尾气,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、混合物分离提纯、气体的制备及实验装置的作用为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
8.在密闭容器中,一定量混合气体发生下列反应:aA(g)+bB(g)?cC(g)+dD(g),达到平衡后,测得C气体的浓度为0.5mol/L.恒温下,将密闭容器的体积缩小为$\frac{1}{2}$,再达平衡时,测得C气体的浓度为0.9mol/L.则下列叙述正确的是( )
| A. | C的体积分数增大 | B. | 平衡向右移动 | C. | B的转化率提高 | D. | a+b<c+d |
10.若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1molNa2O2中含有的离子数为0.4NA | |
| B. | 利用氧化还原反应原理制取1mol氧气,转移的电子数一定为4NA | |
| C. | 7.1g氯气与足量NaOH溶液反应电子转移数为0.2NA | |
| D. | 0.1mol氯气与金属铁完全反应时,转移电子数为0.2NA |
17.2.3g钠在干燥的空气中与O2反应,可得3.5g氧化物,据此可判断其产物为( )
| A. | 只有Na2O | B. | 只有Na2O2 | C. | Na2O和Na2O2 | D. | 无法确定 |
7.某电镀厂在对金属镀件表面除锈、除污过程中,使用了盐酸、氢氧化钠、碳酸钠.该厂经处理后排放的废水含有H+、OH-、Na+、Fe3+、Cu2+、CO32-、Cl-中的几种离子,某中学生环保志愿者小组对该废水中部分成分进行检测,实验步骤及现象如下表所示.请你填写下表中每步实验现象所对应的实验结论.
根据以上信息综合分析:
(1)你推测该废水中除H2O外,还含有的物质是NaOH(写化学式,下同);
(2)不能确定的物质是NaCl.
(3)为了确定可能的物质是否有,应加入的试剂是硝酸、硝酸银.
| 实验步骤及现象 | 实验结论(填离子符号) |
| 取废水样品观察,呈无色 | 废水中不含Cu2+、Fe3+ |
| 测所取废水样品的pH,pH=13 | 废水中含较多的OH- |
| 向废水样品中加入过量的稀盐酸,没有气泡产生 | 废水中不含CO32- |
(1)你推测该废水中除H2O外,还含有的物质是NaOH(写化学式,下同);
(2)不能确定的物质是NaCl.
(3)为了确定可能的物质是否有,应加入的试剂是硝酸、硝酸银.
12.下列化学用语正确的是( )
| A. | 8个中子的碳原子的核素符号:12C | B. | 次氯酸的结构式:H-Cl-O | ||
| C. | 氢氧根离子的电子式: | D. | Cl-离子结构示意图: |
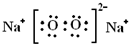 .
.

 ;
;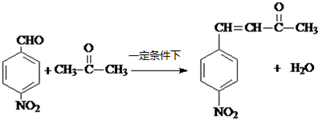 ;
;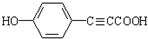 ;
;