题目内容
对于某些离子的检验及结论一定正确的是( )
| A、加入盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- |
| B、加入AgNO3溶液,生成白色沉淀,加稀硝酸沉淀不溶解,说明含有Cl- |
| C、加入氯化钡有白色沉淀,再加盐酸,沉淀不消失,一定有SO42- |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
考点:常见阳离子的检验,常见阴离子的检验
专题:
分析:A、碳酸根离子、碳酸氢根离子均可以和盐酸反应产生二氧化碳;
B、氯化银不溶于硝酸;
C、可能为Ag+;
D、可能为BaCO3、CaCO3、MgCO3等白色沉淀.
B、氯化银不溶于硝酸;
C、可能为Ag+;
D、可能为BaCO3、CaCO3、MgCO3等白色沉淀.
解答:
解:A、加入稀盐酸产生无色气体,可以是二氧化碳、二氧化硫,含有的离子可以是碳酸根、碳酸氢根、亚硫酸根、亚硫酸氢根离子等,故A错误;
B、氯化银不溶于硝酸,加入AgNO3溶液,生成白色沉淀,加稀硝酸沉淀不溶解,说明含有Cl-,故B正确;
C、加入氯化钡有白色沉淀,再加盐酸,沉淀不消失,可能为Ag+,AgCl也不溶于盐酸,故C错误;
D、可能为BaCO3、CaCO3、MgCO3等白色沉淀,所以不一定为Ba2+,故D错误.
故选B.
B、氯化银不溶于硝酸,加入AgNO3溶液,生成白色沉淀,加稀硝酸沉淀不溶解,说明含有Cl-,故B正确;
C、加入氯化钡有白色沉淀,再加盐酸,沉淀不消失,可能为Ag+,AgCl也不溶于盐酸,故C错误;
D、可能为BaCO3、CaCO3、MgCO3等白色沉淀,所以不一定为Ba2+,故D错误.
故选B.
点评:本题考查物质的检验、鉴别,题目难度中等,注意把握可能出现的干扰离子,熟练掌握常见离子的性质是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用下列装置不能达到有关实验目的是( )
A、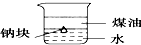 证明ρ(煤油)<ρ(钠)<ρ(水) |
B、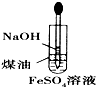 制备Fe(OH)2 |
C、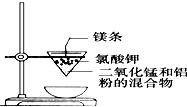 制取金属锰 |
D、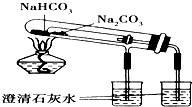 比较NaHCO3和Na2CO3的热稳定性 |
用简便的方法鉴别硫酸铜、碳酸钠、氢氧化镁三种白色固体粉末,应选用的最佳试剂是( )
| A、稀盐酸 | B、紫色石蕊试液 |
| C、水 | D、氢氧化钠溶液 |
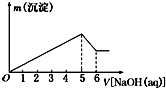 向某硫酸铝和硫酸镁的混合溶液中逐滴加入2mol?L-1的NaOH溶液,生成沉淀的质量m与加入NaOH溶液体积的关系如图所示,则原混合溶液中MgSO4与Al2(SO4)3的物质的量浓度之比为( )
向某硫酸铝和硫酸镁的混合溶液中逐滴加入2mol?L-1的NaOH溶液,生成沉淀的质量m与加入NaOH溶液体积的关系如图所示,则原混合溶液中MgSO4与Al2(SO4)3的物质的量浓度之比为( )| A、1:1 | B、1:2 |
| C、1:3 | D、2:1 |
已知;HCN的K=4.9×10-10,H2CO3的K1=4.3×10-7,K2=5.6×10-11.判断等浓度的NaCN、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| A、c(CN-)>c(HCO3-)>c(OH-)>c(H+) |
| B、c (CO32-)>c(CN-)>c(OH-)>c(H+) |
| C、c(CN-)+c(HCN)=c(H2CO3)+c(HCO3-)+c(CO32-) |
| D、c(Na+)+c(H+)=c(CN-)+c(HCO3-)+c(OH-)+c(CO32-) |
等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)=2Z(g)+W(s)△H<0,下列叙述正确的是( )
| A、达到平衡后,降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数 |
| B、达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动 |
| C、达到平衡时,反应速率v正(X)=2v逆(Z) |
| D、平衡常数K值越大,X的转化率越大 |
下列说法正确的是( )
| A、pH=2的HCl溶液和pH=12的NaOH溶液等体积混合,溶液一定显中性 |
| B、水在0.1mol/L CH3COOH溶液中的电离程度比在0.01mol/L CH3COOH溶液中大 |
| C、0.1mol/L的NH4Cl溶液比0.01mol/L的NH4Cl溶液酸性强 |
| D、0.1mol/L的CH3COOH中,H+的物质的量小于0.1mol |
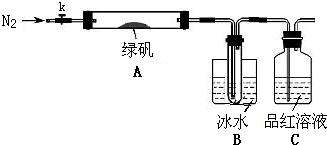 某学习小组拟通过实验探究绿矾(FeSO4?7H2O)热分解的产物.
某学习小组拟通过实验探究绿矾(FeSO4?7H2O)热分解的产物.