题目内容
8.锻烧质量分数为85%的石灰石10kg,在标准状况下,能制得CO2多少立方米?若实际制得CO2 1.5m3,产率是多少?若制得相同体积CO2实际用去10.8kg石灰石,求原料的利用率.分析 据CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,根据方程式中石灰石的质量进行计算;据产率=$\frac{实际产量}{理论产量}$×100%;据利用率=$\frac{实际用量}{投料}$×100%.
解答 解:m(CaCO3)=85%×10kg=8500g
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 g 22.4L
8500g 1904L
则:V(CO2)=1904L=1.904m3
答:能制得1.904m3CO2.
w=$\frac{实际产量}{理论产量}$×100%=$\frac{1.5{m}^{3}}{1.904{m}^{3}}$×100%=78.78%
答:产率是78.78%.
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 22.4
6696 1500
则:m(CaCO3)=6696g=6.696kg
w=$\frac{实际用量}{投料}$×100%=$\frac{6.696kg}{10.8kg}$×100%=62%
答:原料的利用率62%.
点评 正确书写碳酸钙高温煅烧的方程式是本题解题的关键,并注意L和m3之间的换算,本题题目难度中等.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
18.表是元素周期表的一部分,回答下列问题:
(1)元素②的名称为氮,元素⑧的符号为Si.
(2)上述元素中,非金属性最强的元素符号为F,酸性最强的最高价氧化物对应的水化物的化学式为HClO4,能形成两性氢氧化物的元素的符号为Al.
(3)从⑤到⑪的元素中,原子半径最小的元素的符号为Cl.
(4)设计实验证明⑤的单质活动性比⑥的单质活动性强(简述操作过程、现象和结论)将少量Na和Mg分别投入冷水中,金属Na能与水发生剧烈反应,而金属镁反应缓慢,说明Na比Mg活泼.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | O |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑫ | ⑬ |
(2)上述元素中,非金属性最强的元素符号为F,酸性最强的最高价氧化物对应的水化物的化学式为HClO4,能形成两性氢氧化物的元素的符号为Al.
(3)从⑤到⑪的元素中,原子半径最小的元素的符号为Cl.
(4)设计实验证明⑤的单质活动性比⑥的单质活动性强(简述操作过程、现象和结论)将少量Na和Mg分别投入冷水中,金属Na能与水发生剧烈反应,而金属镁反应缓慢,说明Na比Mg活泼.
3.W、X、Y、Z分别为原子序数递增的短周期元素,X、Y的阳离子与Ne具有相同的电子层结构,且其单质均可与水反应,生成W的单质;Z的单质为黄绿色气体.下列说法正确的是( )
| A. | W与X形成的简单二元化合物的电子式为 | |
| B. | 短周期元素中Y的原子半径最大 | |
| C. | 工业上通过电解Y的氧化物制取Y的单质 | |
| D. | 最外层电子数等于其电子层数的金属与Z形成离子化合物 |
13.下列说法正确的是( )
| A. | 分子式为C5H11CI的有机物,分子结构中含2个甲基的同分异构体有4种 | |
| B. | CH3COOH与C2H518OH在浓硫酸作用下加热,反应生有机物分子的结构简式为CH3COOC2H5 | |
| C. | 三氯甲烷只有一种结构,不存在同分异构,证明甲烷是正四面体构型 | |
| D. | 煎炸食物的花生油和牛油都是可皂化的饱和醋类 |
20.下列各原子或离子的电子排布式错误的是( )
| A. | K+ 1s22s22p63s23p6 | B. | F 1s22s22p5 | ||
| C. | S2- 1s22s22p63s23p4 | D. | Ar 1s22s22p63s23p6 |
17.1摩尔丙烷在光照情况下,最多可以与几摩尔氯气发生取代反应( )
| A. | 4mol | B. | 8mol | C. | 10mol | D. | 2mol |
17. 5种固体物质A、B、C、D、E由表中不同的阴阳离子组成,它们均易溶于水.
5种固体物质A、B、C、D、E由表中不同的阴阳离子组成,它们均易溶于水.
分别取它们的水溶液进行实验,结果如下:①A溶液与C溶液混合后产生蓝色沉淀,向该沉淀中加入足量稀HNO3,沉淀部分溶解,剩余白色固体;②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④B溶液与D溶液混合后无现象;
⑤将38.4g Cu片投入装有足量D溶液的试管中,Cu片不溶解,再滴加1.6mol•L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断A、C的化学式为:ACuSO4;CBa(OH)2.
(2)写出步骤②中发生反应的化学方程式2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑.
(3)D溶液中滴入石蕊试液,现象是由无色变成红色,原因是Al3++3H2O?Al(OH)3+3H+(用离子方程式说明).
(4)步骤⑤中若要将Cu片完全溶解,至少加入稀H2SO4的体积是500mL.
(5)现用500mL 3mol•L-1的E溶液充分吸收11.2L CO2气体(标准状况 下),反应后溶液中各离子的物质量浓度由小到大的顺序为c(H+)<c(OH-)<c(CO32-)<c(HCO3-)<c(Na+).
(6)若用惰性电极电解A和B的混合溶液,溶质的物质的量均为0.1mol,请在坐标系中画出通电后阳极产生气体的体积(标准状况下)V与通过电子的物质的量n的关系(不考虑气体溶于水).
 5种固体物质A、B、C、D、E由表中不同的阴阳离子组成,它们均易溶于水.
5种固体物质A、B、C、D、E由表中不同的阴阳离子组成,它们均易溶于水.| 阳离子 | Na+ Al3+Fe3+ Cu2+、Ba2+ |
| 阴离子 | OH- Cl- CO32- NO3- SO4- |
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④B溶液与D溶液混合后无现象;
⑤将38.4g Cu片投入装有足量D溶液的试管中,Cu片不溶解,再滴加1.6mol•L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断A、C的化学式为:ACuSO4;CBa(OH)2.
(2)写出步骤②中发生反应的化学方程式2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑.
(3)D溶液中滴入石蕊试液,现象是由无色变成红色,原因是Al3++3H2O?Al(OH)3+3H+(用离子方程式说明).
(4)步骤⑤中若要将Cu片完全溶解,至少加入稀H2SO4的体积是500mL.
(5)现用500mL 3mol•L-1的E溶液充分吸收11.2L CO2气体(标准状况 下),反应后溶液中各离子的物质量浓度由小到大的顺序为c(H+)<c(OH-)<c(CO32-)<c(HCO3-)<c(Na+).
(6)若用惰性电极电解A和B的混合溶液,溶质的物质的量均为0.1mol,请在坐标系中画出通电后阳极产生气体的体积(标准状况下)V与通过电子的物质的量n的关系(不考虑气体溶于水).
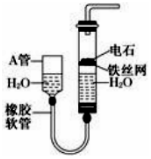 如图,图中的实验装置可用于制取乙炔.
如图,图中的实验装置可用于制取乙炔. 太阳能电池的发展已经进入了第三代.第三代就是铜铟镓硒CIGS等化合物薄膜太阳能电池以及薄膜硅系太阳能电池.完成下列填空:
太阳能电池的发展已经进入了第三代.第三代就是铜铟镓硒CIGS等化合物薄膜太阳能电池以及薄膜硅系太阳能电池.完成下列填空: