题目内容
19.标准状况下,22g CO2的体积是( )| A. | 不能确定 | B. | 11.2 L | C. | 22.4 L | D. | 5.6 L |
分析 根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$计算.
解答 解:标准状况下,22g CO2的物质的量为n=$\frac{m}{M}$=$\frac{22g}{44g/mol}$=0.5mol,则V=nVm=0.5mol×22.4L/mol=11.2L;
故选B.
点评 本题考查物质量的计算,侧重于学生的计算能力的考查,注意相关计算公式的运用,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.NA为阿伏加德罗常数,下列有关说法中不正确的是( )
| A. | 标准状况下,22.4L氦气含有NA个氦原子 | |
| B. | 20g重水含有10 NA个电子 | |
| C. | 12.5mL l6mol•L-1浓硫酸与足量铜反应,转移电子数为0.2NA | |
| D. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
10.下列关于CaCO3的叙述错误的是( )
| A. | CaCO3俗名石灰石,属于碳酸盐 | |
| B. | CaCO3属于含氧酸盐 | |
| C. | 实验室用煅烧CaCO3来制备二氧化碳 | |
| D. | CaCO3 属于难溶性的钙盐 |
7.设NA为阿佛加德罗常数的值,下列说法正确的是( )
| A. | 在标准状况下,22.4L H2O的分子数为NA | |
| B. | 48g O3气体含有NA个O3分子 | |
| C. | 0.5mol•L-1 AlCl3溶液中含有0.5NA个Al3+ | |
| D. | 1molMg变为Mg2+时失去的电子数目为NA |
14.下列离子方程式书写正确的是( )
| A. | 金属铝加到硝酸汞溶液中:2Al+3Hg2+═2Al3++3Hg | |
| B. | 硫酸与氢氧化钡溶液混合:Ba2++OH-+H++SO${\;}_{4}^{2-}$═BaSO4↓+H2O | |
| C. | 饱和石灰水跟稀硝酸反应:Ca(OH)2+2H+═Ca2++2H2O | |
| D. | 碳酸钙溶于醋酸中:CaCO3+2H+═Ca2++H2O+CO2↑ |
11.下列实验方法或操作能达到实验目的是( )
| A. | 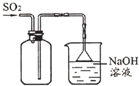 收集SO2 收集SO2 | |
| B. | 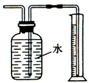 测量Cu与浓硝酸反应生成二氧化氮体积 测量Cu与浓硝酸反应生成二氧化氮体积 | |
| C. | 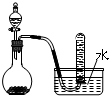 二氧化锰固体和双氧水制取O2 二氧化锰固体和双氧水制取O2 | |
| D. | 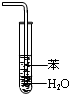 吸收HCl 吸收HCl |
9.表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 在18 g 18O2中含有NA个氧原子 | |
| B. | 1 mol FeI2与足量氯气反应对转移的电子数为2NA | |
| C. | 1 mol Cl2参加反应转移电子数一定为2 NA | |
| D. | 标准状况下,2.24L四氯化碳含有分子数目为0.1NA |